题目内容
17.化学兴趣小组的同学为体验加热固体制取气体的操作步骤和方法,利用6g氯酸钾和2g二氧化锰的混合物加热(化学反应方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑)制取氧气.(1)实验结束后,甲同学认为氯酸钾可能未分解完全,又设计进行了下面的实验:
实验1:将实验加热后的残留物加水至充分溶解,过滤;
实验2:向实验1的滤液中滴加硝酸银溶液至不再产生沉淀,过滤、干燥,称得沉淀质量为5.74g.
小资料:①二氧化锰不溶于水 ②AgClO3易溶于水
甲同学分析实验过程,其中仅涉及两步化学反应:
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ KCl+AgNO3═AgCl↓+KNO3
推出两反应间存在KClO3→KCl→AgCl↓物质转化关系和质量比例关系.
请你利用上述关系,通过计算帮甲同学判断KClO3是否完全分解?KClO3没有完全分解(要求:简单写出计算过程、说明判断依据,计算结果精确到0.1)
(2)乙同学对甲同学的方案提出质疑:认为通过称量加热后残留物质量,利用加热前后质量差进行计算,同样达到甲同学的实验目的.你赞同乙同学的观点吗?说明理由:赞同;由质量守恒定律,固体混合物减少的质量即为生成氧气的质量,由反应的化学方程式计算出参加反应的氯酸钾的质量.
分析 (1)由反应的化学方程式,找出KClO3→KCl→AgCl↓物质转化关系和质量比,由生成沉淀的质量,计算出参加反应的氯酸钾的质量,进而判断KClO3是否完全分解.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,根据质量守恒定律,进行分析解答.
解答 解:(1)由反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑、KCl+AgNO3═AgCl↓+KNO3,则2KClO3~2KCl~2AgCl,即KClO3~KCl~AgCl,它们的质量关系为122.5:74.5:143.5.
设参加反应的氯酸钾的质量为x
KClO3~KCl~AgCl
122.5 143.5
x 5.74g
$\frac{122.5}{143.5}$=$\frac{x}{5.74g}$ x=4.9g
6g>4.9g,故KClO3没有完全分解.
(2)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,通过称量加热后残留物质量,加热前后质量差,即为生成氧气的质量,由生成氧气的质量,由反应的化学方程式列式计算出参加反应的氯酸钾的质量,进而判断是否完全分解.
答:(1)KClO3~KCl~AgCl,质量比为122.5:74.5:143.5;KClO3没有完全分解;(2)赞同;由质量守恒定律,固体混合物减少的质量即为生成氧气的质量,由反应的化学方程式计算出参加反应的氯酸钾的质量.
点评 本题难度不大,掌握根据化学方程式的计算是正确解答本题的关键,解题时要注意解题的规范性.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
7.某合金粉末除含铝外,还含有铁、铜中的一种或两种.已知铝能够与氢氧化钠和水反应生成NaAlO2和一种可燃性气体.现在只用稀硫酸和氢氧化钠溶液来确定该合金的组成.实验记录如表:
请回答:
(1)该合金的组成是Al、Fe、Cu.
(2)①中发生反应的化学方程式为2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(3)②中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑.
| 实验步骤 | 实验现象 |
| ①取一定量的合金粉末,加入过量的氢氧化钠溶液,充分反应后过滤,滤纸上剩余物备用 | 粉末部分溶解,并有无色体放出 |
| ②取步骤①所得固体物质,加入过量的稀硫酸,充分反应 | 固体物质部分溶解,并有无色气体放出,溶液呈浅绿色 |
(1)该合金的组成是Al、Fe、Cu.
(2)①中发生反应的化学方程式为2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(3)②中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑.
8.下列有关物质的用途,利用了物质的物理性质的是( )
| A. | 生石灰用作干燥剂 | B. | 氧气用于医疗急救 | ||
| C. | 用洗洁精洗涤餐具上的油污 | D. | 熟石灰可用于改良酸性土壤 |
5.氯酸(HClO3)中氯元素化合价为( )
| A. | +1 | B. | +3 | C. | +7 | D. | +5 |
2.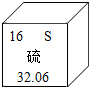 如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )
如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )
 如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )
如图是元素周期表中某元素的相关信息,从图中不能直接获取的信息是( )| A. | 该元素属于非金属元素 | |
| B. | 该元素的原子序数为16 | |
| C. | 该元素的相对原子质量32.06 | |
| D. | 该元素组成的单质常温下是黄色固体 |
6.20℃时,取甲、乙、丙、丁四种纯净物个40g,分别加入到四个各盛有100g水的烧杯中,充分溶解,其溶解情况如表:
下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 未溶解固体的质量/g | 8.4 | 4 | 0 | 18.4 |
| A. | 所得四杯溶液都是饱和溶液 | |
| B. | 丁溶液的溶质质量分数最大 | |
| C. | 20℃时四种物质质溶解度的关系为:丁>甲>乙>丙 | |
| D. | 四杯溶液中各加入20℃的100g水后,溶液质量相等,且均为不饱和溶液 |
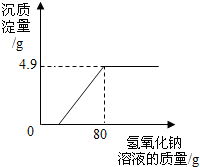 某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算:
某校化学兴趣小组在参加社会实践活动时,环保组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保组的同学进行了以下实验:取废水300g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得沉淀质量与所加入的氢氧化钠溶液的质量关系如图,请分析计算: