题目内容
19.甲、乙两种固体物质的溶解度曲线如图1所示.
(1)图1中P点的含义是20℃时,甲、乙的溶解度均为30g.
(2)40℃时,饱和溶液中溶质的质量分数:甲>乙(填“>”、“=”或“<”).若将40℃的甲、乙的饱和溶液降温至15℃,则饱和溶液中溶质的质量分数:甲<乙(填“>”、“=”或“<”).20℃时,将60g乙物质放入100g水中,升温至40℃,溶液中溶解的溶质与溶剂的质量比为2:5(用最简整数比表示).
(3)20℃时,进行了如图2所示的实验:
上述实验过程中所得的溶液,属于不饱和溶液的是AC(填序号,下同),E溶液与B溶液中溶质的质量分数相同.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,图1中P点的含义是:20℃时,甲、乙的溶解度均为30g;
(2)40℃时,甲物质的溶解度大于乙物质的溶解度,所以饱和溶液中溶质的质量分数:甲>乙,若将40℃的甲、乙的饱和溶液降温至15℃,15℃时,乙物质的溶解度大于甲物质的溶解度,所以饱和溶液中溶质的质量分数:甲<乙,20℃时,将60g乙物质放入100g水中,升温至40℃,40℃时,乙物质的溶解度是40g,所以溶液中溶解的溶质与溶剂的质量比为40g:100g=2:5;
(3)20℃时,甲物质的溶解度是30g,所以100g水中加入20g甲得到的A是不饱和溶液,再加入20gA,得到该温度时的B为饱和溶液;
40℃时,甲物质的溶解度是50g,所以C是不饱和溶液,再加入20g的甲,得到的D为饱和溶液;
降温到20℃,得到该温度的饱和溶液,所以上述实验过程中所得的溶液,属于不饱和溶液的是AC,E溶液与B溶液中溶质的质量分数相同.
故答案为:(1)20℃时,甲、乙的溶解度均为30g;
(2)>,<,2:5;
(3)AC,E.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
9.在金、银、铜、铁、锡五种金属中,与稀硫酸反应最为剧烈的是( )
| A. | 铁 | B. | 金 | C. | 锡 | D. | 铜 |
14.某研究性学习小组的甲、乙两名同学分别从室温的一瓶硝酸钾不饱和溶液中各取出100g和80g,他们将各自所取的溶液恒温蒸发掉20g水后,经测定乙同学所剩余溶液刚好成为室温时的饱和溶液.请分析,此时甲同学所剩余溶液是( )
| A. | 室温的饱和溶液 | |
| B. | 室温时的不饱和溶液 | |
| C. | 室温时的不饱和溶液,且有晶体析出 | |
| D. | 室温时的饱和溶液,且有晶体析出 |
4.下列事实能证明在化学反应中分子可分的是( )
| A. | 浓盐酸长时间敞口放置质量减轻了 | B. | 水蒸气液化成水 | ||
| C. | 水通电可以得到氢气和氧气 | D. | 蔗糖放入水中不见了 |
11.根据所给的化学反应,填写化学方程式,并回答有关问题:
| 化学反应 | 化学方程式 | 简答 |
| 二氧化碳通 入灼热的碳 | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | 反应类型化合反应 |
| 硫在空气中 燃烧 | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | 观察到的现象剧烈燃烧,发出微弱的淡蓝色火焰 |
| 氯酸钾与二 氧化锰共热 | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 加热时试管口应稍微向下倾斜 |
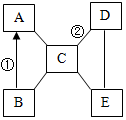 A、B、C、D、E是初中化学常见五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去,回答下列问题:
A、B、C、D、E是初中化学常见五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去,回答下列问题: