题目内容
10.5月18日国务院电贺国土部实现了首次成功试开采“可燃冰”、“可燃冰”也就是我们所说的天然气水合物,其主要成分是甲烷(CH4),按物质类别分甲烷(CH4)属于纯净物(填“混合物”或“纯净物”),甲烷燃烧化学方程式如下:CH4+2O2═X+2H2O,则X的化学式是CO2.分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:甲烷(CH4)是由一种物质组成的,属于纯净物;根据反应的化学方程式可知反应物中碳、氢、氧原子个数分别为1、4、41,反应后的生成物中碳、氢、氧原子个数分别为0、4、2,根据反应前后原子种类、数目不变,则每个X分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2.
故答案为:纯净物;CO2.
点评 本题难度不大,掌握常见物质的元素组成、利用化学反应前后原子守恒来确定物质化学式的方法等是正确解题的关键.

练习册系列答案
 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目
18.下列图象能正确反映其对应变化关系的是( )
| A. | 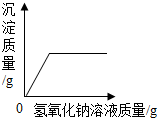 向FeCl3和HNO3的混合溶液中加入NaOH溶液直至过量 | |
| B. | 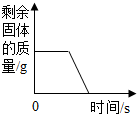 煅烧一定质量的石灰石 | |
| C. | 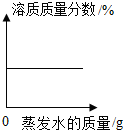 恒温条件下,将足量的饱和硝酸钾溶液蒸发一定质量的水 | |
| D. | 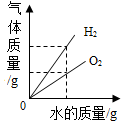 水在通电的条件下反应 |
15.有科学家研究发现,氧气可通过高能真空紫外线照射二氧化碳直接产生,该化学反应模型如图所示.关于该反应的说法不正确的是( )
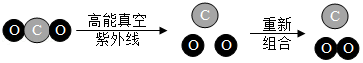

| A. | 符合质量守恒定律 | B. | 化学反应中的最小微粒是原子 | ||
| C. | 属于化合反应 | D. | 为制取氧气提供了新方法 |



 A、B、C、D、E、F、G、H八种物质,有如图所示的反应关系,其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E、F是无色液体,H是一种能使澄清石灰水变浑浊的气体.试推断:
A、B、C、D、E、F、G、H八种物质,有如图所示的反应关系,其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E、F是无色液体,H是一种能使澄清石灰水变浑浊的气体.试推断: