题目内容
黑白复印机用的墨粉中常添加Fe3O4粉末,Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的.如图是氧化沉淀法生产复印用Fe3O4粉末的流程简图.已知第④步反应中各元素化合价保持不变.
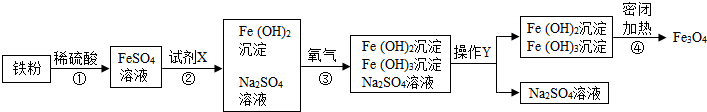
(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是 色.
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为 .
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于 ,才能确保最终生成Fe3O4,操作Y的名称为 .

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是
(2)第②步加入试剂X,生成Fe(OH)2的反应方程式为
(3)在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于
考点:物质的相互转化和制备,过滤的原理、方法及其应用,金属的化学性质,化学性质与物理性质的差别及应用,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据四氧化三铁的物理性质进行分析;
(2)根据题中的反应原理找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
(3)根据Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的,然后依据氢氧化亚铁和氧气反应的方程式进行分析;
根据过滤操作可以将固体和液体分离进行分析.
(2)根据题中的反应原理找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
(3)根据Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的,然后依据氢氧化亚铁和氧气反应的方程式进行分析;
根据过滤操作可以将固体和液体分离进行分析.
解答:解:(1)四氧化三铁是黑色的固体,而Fe3O4粉末在复印机的电磁场作用下能使墨粉形成黑色的字迹或图案,所以还利用了Fe3O4是黑色;
(2)通过题中的反应原理可以看出,硫酸亚铁和试剂X反应生成了氢氧化亚铁和硫酸钠溶液,结合复分解反应的原理可知,X是氢氧化钠溶液,氢氧化钠溶液和硫酸亚铁反应生成了硫酸钠和氢氧化亚铁沉淀,
化学方程式为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;
(3)Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的,依据质量守恒定律可知,通入氧气后生成的氢氧化亚铁和氢氧化铁的个数比是:1:2,所以生成的Fe(OH)2和Fe(OH)3的质量比等于:(56+17×2):2×(56+17×3)=45:107,经过操作Y后,得到了氢氧化铁沉淀、氢氧化亚铁沉淀和硫酸钠溶液,所以操作Y的名称为:过滤.
故答案为:(1)黑;
(2)FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;
(3)45:107,过滤.
(2)通过题中的反应原理可以看出,硫酸亚铁和试剂X反应生成了氢氧化亚铁和硫酸钠溶液,结合复分解反应的原理可知,X是氢氧化钠溶液,氢氧化钠溶液和硫酸亚铁反应生成了硫酸钠和氢氧化亚铁沉淀,
化学方程式为:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;
(3)Fe3O4是由Fe2+、Fe3+和O2-按1:2:4的个数比构成的,依据质量守恒定律可知,通入氧气后生成的氢氧化亚铁和氢氧化铁的个数比是:1:2,所以生成的Fe(OH)2和Fe(OH)3的质量比等于:(56+17×2):2×(56+17×3)=45:107,经过操作Y后,得到了氢氧化铁沉淀、氢氧化亚铁沉淀和硫酸钠溶液,所以操作Y的名称为:过滤.
故答案为:(1)黑;
(2)FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;
(3)45:107,过滤.
点评:在解此类题时,首先分析题中的反应原理,然后结合题中所给的知识和学过的知识逐一的进行解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、用灼烧的方法可以鉴别羊毛和棉纶 |
| B、KMnO4和K2MnO4中的锰元素化合价相同 |
| C、用水除去氧化钙中的碳酸钙 |
| D、用活性炭吸附的方法鉴别硬水和软水 |
 氢氧化钠露置在空气中会变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
氢氧化钠露置在空气中会变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题: 小明探究“不同物质的吸热能力”时,在两支相同的试管中分别装入质量相等、温度相同的水和煤油,用一个酒精灯同时对两支试管加热,加热一段时间后,温度计示数如图所示.
小明探究“不同物质的吸热能力”时,在两支相同的试管中分别装入质量相等、温度相同的水和煤油,用一个酒精灯同时对两支试管加热,加热一段时间后,温度计示数如图所示.