题目内容
 氢氧化钠露置在空气中会变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
氢氧化钠露置在空气中会变质,现称取变质的氢氧化钠样品10g,配制成溶液,再向其中加入CaCl2溶液,反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:(1)恰好完全反应时烧杯中溶液的pH
(2)计算样品中NaOH的质量;
(3)计算所加CaCl2溶液的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:氢氧化钠能和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,根据碳酸钙沉淀的质量可以计算碳酸钠的质量和氯化钙的质量,根据碳酸钠的质量可以计算样品中NaOH的质量,根据氯化钙的质量、氯化钙溶液的质量可以计算所加CaCl2溶液的溶质质量分数.
解答:解:(1)恰好完全反应时烧杯中的溶液中含有氢氧化钠和氯化钠,氯化钠溶液显中性,氢氧化钠溶液显碱性,因此溶液显碱性,pH>7.
故填:>.
(2)设样品中碳酸钠的质量为x,反应的氯化钙的质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 111 100
x y 5g
=
=
,
x=5.3g,y=5.55g,
样品中NaOH的质量为:10g-5.3g=4.7g,
答:样品中NaOH的质量为4.7g.
(3)所加CaCl2溶液的溶质质量分数为:
×100%=11.1%,
答:所加CaCl2溶液的溶质质量分数为11.1%.
故填:>.
(2)设样品中碳酸钠的质量为x,反应的氯化钙的质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 111 100
x y 5g
| 106 |
| x |
| 111 |
| y |
| 100 |
| 5g |
x=5.3g,y=5.55g,
样品中NaOH的质量为:10g-5.3g=4.7g,
答:样品中NaOH的质量为4.7g.
(3)所加CaCl2溶液的溶质质量分数为:
| 5.55g |
| 50g |
答:所加CaCl2溶液的溶质质量分数为11.1%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列各组离子中,能在pH=12的溶液中大量共存的是( )
| A、Na+、Ca2+、Cl-、CO32- |
| B、NH4+、NO3-、K+、CO32- |
| C、K+、Ba2+、Cl-、SO42- |
| D、Na+、Ba2+、Cl-、NO3- |
某白色固体甲,可能含有硫酸钠、氢氧化钠、碳酸钠、氯化钠中的一种或几种;某无色溶液乙是初中化学常见的一种可溶性钡盐溶液.为探究它们的成分,进行如图实验.对于固体甲的分析正确的是( )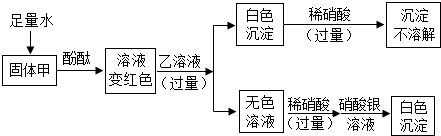

| A、不一定有硫酸钠 |
| B、一定有氢氧化钠 |
| C、一定有氯化钠 |
| D、至少含有碳酸钠、氢氧化钠中的一种 |
下列有关物质用途的说法,不正确的是( )
| A、纯碱用于造纸,纺织、洗涤剂的生产等 |
| B、氢氧化钠用于改良酸性土壤 |
| C、碳酸钙用做建筑材料 |
| D、农业上常用硫酸铁配制波尔多液 |