题目内容
15.100吨含Fe2O3质量分数为85%的铁矿石中,可炼出含铁质量分数为96%的生铁为多少吨?( 结果取整数)分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:设可炼出含铁质量分数为96%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
100t×85% 96%x
$\frac{160}{112}=\frac{100t×85%}{96%x}$ x≈62t
答:可炼出含铁质量分数为96%的生铁的质量为62t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.某校科学兴趣小组探究城市中不同场所CO2含量的高低,他们实验步骤和数据如下:
a.配制测试试剂:
取烧杯一只,加入蒸馏水,滴加酚酞溶液1~3滴,边搅拌,边滴加稀氨水(一种碱溶液),直到溶液变红色,将溶液倒到细口瓶中密封保存.
b.选定测试采样点(选定的测试采样点见表).
c.CO2的相对含量的测定:
用50毫升医用注射器吸取上面配制好的溶液10毫升,在一个采样点抽气到50毫升刻度线处,用食指堵住注射器的吸入口,用力震荡注射器2~3分钟,然后将注射器的吸入口向上,小心地将剩余气体排出.继续上述操作,直到注射器内的溶液红色恰好褪去.在表中记下抽气的次数.
d.同一天,在其它选定的采样点,用相同的方法操作,进行测定,记录下抽气的次数.(三次居民区的采样点是同一地点)
e.处理数据,并以操场空气中CO2的含量为标准值进行对照.
请回答下列问题:
(1)测试时,注射器中溶液的pH 变小,当注射器内的溶液红色恰好褪去时,溶液中肯定存在的物质是盐.(选填“酸”、“碱”或“盐”)
(2)根据以上测试数据可以得出的结论是哪个场所的CO2含量最高车站.
a.配制测试试剂:
| 编号 | 取样 地点 | 取样时间 | 抽气次数 |
| 1 | 操场 | 17:30 | 16 |
| 2 | 居民区 | 9:10 | 8 |
| 3 | 居民区 | 13:15 | 7 |
| 4 | 居民区 | 17:55 | 5 |
| 5 | 公园 | 12:35 | 7 |
| 6 | 车站 | 16:45 | 4 |
| 7 | 酒店 | 17:50 | 5 |
b.选定测试采样点(选定的测试采样点见表).
c.CO2的相对含量的测定:
用50毫升医用注射器吸取上面配制好的溶液10毫升,在一个采样点抽气到50毫升刻度线处,用食指堵住注射器的吸入口,用力震荡注射器2~3分钟,然后将注射器的吸入口向上,小心地将剩余气体排出.继续上述操作,直到注射器内的溶液红色恰好褪去.在表中记下抽气的次数.
d.同一天,在其它选定的采样点,用相同的方法操作,进行测定,记录下抽气的次数.(三次居民区的采样点是同一地点)
e.处理数据,并以操场空气中CO2的含量为标准值进行对照.
请回答下列问题:
(1)测试时,注射器中溶液的pH 变小,当注射器内的溶液红色恰好褪去时,溶液中肯定存在的物质是盐.(选填“酸”、“碱”或“盐”)
(2)根据以上测试数据可以得出的结论是哪个场所的CO2含量最高车站.
20.氢氧化钠是工业生产和生活的一种重要原料,也是实验室里常见的一种药品.下表是20℃时,氢氧化钠溶解于水的实验数据,回答下列问题:
(1)计算第2次实验得到的氢氧化钠溶液的溶质质量分数.
(2)m=15.1
(3)在这4次实验中,得到的氢氧化钠溶液属于饱和溶液的是③④(填实验序号)
| 实验序号 | 水的质量(克) | 加入氢氧化钠的质量(克) | 溶液的质量(克) |
| ① | 10 | 4 | 14 |
| ② | 10 | 5 | 15 |
| ③ | 10 | 6 | 15.1 |
| ④ | 10 | 7 | m |
(2)m=15.1
(3)在这4次实验中,得到的氢氧化钠溶液属于饱和溶液的是③④(填实验序号)
7.在托盘天平两端各放一只烧杯,调节至平衡,向烧杯里分别注入等质量、等质量分数的硫酸溶液,然后向一只烧杯里加入一定质量的镁,向另一只烧杯里加入等质量的铜铝合金,两烧杯中的反应恰好完全,且天平仍保持平衡,铜铝合金中铜与铝的质量比是( )
| A. | 1:3 | B. | 1:2 | C. | 3:4 | D. | 2:3 |
4.化学符号“2H”表示的正确的意义是( )
| A. | 2个氢分子 | B. | 2个氢原子 | C. | 2个氢元素 | D. | 2克氢元素 |
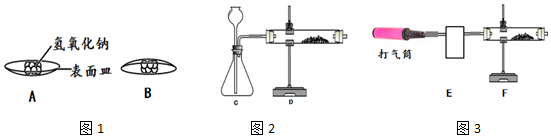
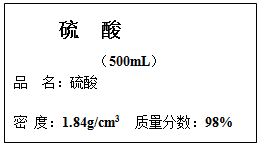 如图是学校实验室中硫酸试剂的标签,请阅读后计算下列试题.
如图是学校实验室中硫酸试剂的标签,请阅读后计算下列试题.