题目内容
10.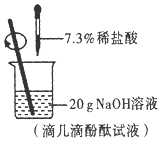 将溶质质量分数为7.3%的稀盐酸滴入盛有20g氢氧化钠溶液(滴有几滴酚酞试液,如图所示)的烧杯中,恰好完全反应时消耗稀盐酸50g.
将溶质质量分数为7.3%的稀盐酸滴入盛有20g氢氧化钠溶液(滴有几滴酚酞试液,如图所示)的烧杯中,恰好完全反应时消耗稀盐酸50g.试回答:
(1)恰好完全反应时烧杯中的现象是液体由红色恰好变为无色.
(2)计算所用氢氧化钠溶液的溶质质量分数.
分析 稀盐酸与氢氧化钠溶液反应生成氯化钠和水,由参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式列式计算出参加反应的氢氧化钠的质量,进而计算出氢氧化钠溶液的溶质质量分数.
解答 解:(1)氢氧化钠溶液呈碱性,能使酚酞试液变红,当氢氧化钠和盐酸恰好完全反应时,烧杯中的液体由红色恰好变为无色,故填:液体由红色恰好变为无色;
(2)消耗盐酸溶液中溶质质量为:50g×7.3%=3.65g
设氢氧化钠溶液中溶质质量为x
HCl+NaOH═NaCl+H2O
36.5 40
3.65g x
$\frac{36.5}{40}=\frac{3.65g}{x}$
x=4g
故氢氧化钠溶液的溶质质量分数为:$\frac{4g}{20g}×100%$=20%
答:所用氢氧化钠溶液的溶质质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列属于化学变化的是( )
| A. | 冰雪融化 | B. | 瓷器破碎 | C. | 牛奶变酸 | D. | 酒精挥发 |
18.下列做法是为了隔绝空气中氧气的是( )
| A. | 木制家具表面喷漆 | B. | 油锅着火立即盖上锅盖 | ||
| C. | 澄清石灰水密封保存 | D. | 食品放入冰箱中冷藏 |
5.如表是KCl的部分溶解度数据,下列说法正确的是( )
| 温度(℃) | 0 | 20 | 40 | 60 |
| 溶解度(g) | 27.6 | 34 | 40 | 45.5 |
| A. | 20℃时,100g KCl饱和溶液中含KCl 34g | |
| B. | 任何温度下的KCl饱和溶液都不能再溶解其它物质 | |
| C. | 40℃的KCl溶液的浓度一定大于20℃的KCl饱和溶液的浓度 | |
| D. | 将60℃的KCl溶液降温至40℃时,不一定有晶体析出 |
15.“经常用脑,多喝六个核桃”,核桃中所含的脂肪主要成分是亚油酸甘油脂(C21H38O4),可供给大脑基质的需要,下列说法正确的是( )
| A. | 亚油酸甘油酯中含有63个原子 | |
| B. | 亚油酸甘油酯中碳、氢的质量比为21:38 | |
| C. | 亚油酸甘油酯中含氢的质量分数最高 | |
| D. | 亚油酸甘油酯属于有机物 |
 2016年9月15日,我国在酒泉卫星发射中心用长征二号F运载火箭将天宫二号空间实验室发射升空.长征二号F运载火箭是目前我国所有运载火箭中长度最长的火箭,如图是长征二号F运载火箭图片,请回答有关问题.(1)逃逸发动机尾喷管、逃逸塔和电器控制系统等多处关键部件都使用优质钢材,钢属于金属材料(选填“金属材料”或“有机合成材料”).
2016年9月15日,我国在酒泉卫星发射中心用长征二号F运载火箭将天宫二号空间实验室发射升空.长征二号F运载火箭是目前我国所有运载火箭中长度最长的火箭,如图是长征二号F运载火箭图片,请回答有关问题.(1)逃逸发动机尾喷管、逃逸塔和电器控制系统等多处关键部件都使用优质钢材,钢属于金属材料(选填“金属材料”或“有机合成材料”).