题目内容
9.下面是甲、乙两同学在学完酸的化学性质后所做的实验:
【观察与讨论一】甲同学在两物质充分反应后,再滴加无色酚酞溶液,无明显现象(已知CaCl2溶液呈中性).
【观察与讨论二】乙同学在做实验时开始没有观察到气泡产生,于是对碳酸钠能否与盐酸反应表示怀疑.
在碳酸钠溶液中滴加很少量稀盐酸时,先发生反应Na2CO3+HCl═NaCl+NaHCO3,继续滴加稀盐酸,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑.所以他认为,实验时还应继续加入稀盐酸,才能观察到有气泡产生.
【观察与讨论三】甲同学先将废液缓慢倒入一洁净的废液杯中,乙同学在观察到气泡产生后,也将实验废液缓慢倒入该废液杯中,没有观察到明显现象,经过讨论确定,甲同学的试管废液中含有的溶质一定有CaCl2(填化学式,下同),乙同学的试管废液中含有的溶质一定有NaCl.为了处理实验后产生的废液,甲、乙同学决定对废液杯中最终废液溶质的成分进行探究,
【提出问题】最终废液中含有什么溶质?
【猜想与假设】猜想1:废液中含有CaCl2、NaCl两种溶质.
猜想2:废液中含有CaCl2、NaCl、HCl三种溶质.
猜想3:废液中含有NaHCO3、CaCl2、NaCl三种溶质.
【活动与探究】甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生.
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色.
【结论与反思】(1)猜想2(填“1”或“2”或“3”)正确.
(2)要得到相同的结论,还可采用很多种方法.如加入氧化铁粉末,可观察到溶液呈黄色,该反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O.
分析 【观察与讨论2】根据只有当稀盐酸足量时,碳酸钠溶液才能够和稀盐酸反应生成二氧化碳进行分析;
【观察与讨论3】无论氢氧化钙和稀盐酸是否恰好完全反应,形成的溶液中一定含有氯化钙;
无论碳酸钠和稀盐酸的质量如何,形成的溶液中一定含有氯化钠;
【猜想与假设】如果物质之间恰好完全反应时,废液中含有氯化钙和氯化钠;
如果稀盐酸过量时,废液中含有氯化钙、氯化钠和氯化氢;
如果稀盐酸不足,废液中含有碳酸氢钠、氯化钙和氯化钠;
【结论与反思】根据实验现象可以判断废液中溶质的组合情况;
根据氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的进行分析.
解答 解:【观察与讨论2】只有当稀盐酸足量时,碳酸钠溶液才能够和稀盐酸反应生成二氧化碳,所以乙同学实验时还应继续加入稀盐酸,才能观察到有气泡产生;
【观察与讨论3】无论氢氧化钙和稀盐酸是否恰好完全反应,形成的溶液中一定含有氯化钙;无论碳酸钠和稀盐酸的质量如何,形成的溶液中一定含有氯化钠,所以甲同学的试管中废液含有的溶质一定有氯化钙,化学式是CaCl2;乙同学的试管中废液含有的溶质一定有氯化钠,化学式是NaCl;
【猜想与假设】猜想1:废液中含有CaCl2、NaCl两种溶质;
猜想2:废液中含有CaCl2、NaCl、HCl三种溶质;
【结论与反思】(1)由以上分析可知,猜想2正确;
(2)要得到相同的结论,还可采用很多种方法.如加入氧化铁粉末,氧化铁和盐酸反应生成氯化铁和水,可观察到溶液呈黄色,化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
故答案为:【观察与讨论2】继续加入稀盐酸;
【观察与讨论3】CaCl2;NaCl;
【猜想与假设】猜想1:CaCl2、NaCl;
猜想2:CaCl2、NaCl、HCl;
【结论与反思】(1)2;
(2)黄,Fe2O3+6HCl═2FeCl3+3H2O.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 水体富营养化:水中氮、磷等物质含量过高 | |
| B. | 酸雨:CO、CO2的排放 | |
| C. | 雾霾:工业废气、汽车尾气、道路扬尘等 | |
| D. | 臭氧层空洞;氟利昂等排放 |
| A. | 某固体中加入稀盐酸,产生了无色气体,证明该固体一定含有CO32- | |
| B. | 某无色溶液滴加酚酞试液显红色,该溶液不一定是碱 | |
| C. | 打开盛放浓盐酸的试剂瓶瓶塞,瓶口产生白雾,所以打开盛放浓硫酸的试剂瓶瓶塞,也能看见白雾 | |
| D. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
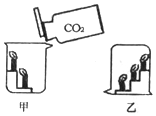 如图所示,甲烧杯中有高低两支燃烧的蜡烛,沿烧杯壁向烧杯中倾倒二氧化碳,乙图有三支高低燃烧的蜡烛,被罩在一只稍大一些的烧杯中,对甲、乙中蜡烛燃烧的现象描述正确的是( )
如图所示,甲烧杯中有高低两支燃烧的蜡烛,沿烧杯壁向烧杯中倾倒二氧化碳,乙图有三支高低燃烧的蜡烛,被罩在一只稍大一些的烧杯中,对甲、乙中蜡烛燃烧的现象描述正确的是( )| A. | 甲、乙都是自下而上依次熄灭 | |
| B. | 甲、乙都是自上而下依次熄灭 | |
| C. | 甲中自上而下依次熄灭,乙中自下而上依次熄灭 | |
| D. | 甲中自下而上依次熄灭,乙中自上而下依次熄灭 |
| A. |  | B. |  | C. |  | D. |  |
| A. | 石油是不可再生资源 | |
| B. | 将石油分馏可以得到多种产品 | |
| C. | 石油是理想的、清洁的燃料 | |
| D. | 石油不充分燃烧会生成一氧化碳等有害物质 |
| A. | 墙内开花墙外香--微粒在不断的运动 | |
| B. | 给轮胎打气--气体微粒空隙较大 | |
| C. | 热胀冷缩--温度越高微粒越大 | |
| D. | 一滴水约含1.67×1021个水分子--微粒很小 |


