题目内容
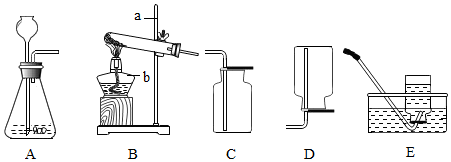
20.根据下列气体制取的实验装置图,回答问题:
(1)请写出仪器名称:①是试管,②是水槽
(2)实验室制取CO2的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,应选择的气体发生装置是B(填序号,下同),气体收集装置是C.将制得的二氧化碳气体通入新制的澄清石灰水中,始终未出现浑浊现象,可能的原因是二氧化碳中含有氯化氢气体
(3)实验室加热氯酸钾和二氧化锰制取氧气应选择的发生装置是A,若用盛满水的F装置收集氧气,则氧气应从导管口b(填“a”或“b”)通入
(4)常温下氨气(NH3)是一种无色、有刺激性气味、密度比空气小、极易溶于水的气体,实验室常用氯化铵固体与碱石灰固体共热来制取氨气,则实验室制取并收集氨气应选择的装置组合是AD.
分析 试管是常用的反应容器,水槽是常用的盛水的仪器;制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.将制得的二氧化碳气体通入新制的澄清石灰水中,始终未出现浑浊现象,可能的原因是:二氧化碳中含有氯化氢气体;如果用氯酸钾制氧气就需要加热,若用盛满水的F装置收集氧气,则氧气应从导管口b端进入,因为氧气的密度比水小;实验室常用氯化铵固体与碱石灰固体共热来制取氨气,因此需要加热;常温下氨气(NH3)是一种无色、有刺激性气味、密度比空气小、极易溶于水的气体,因此只能用向下排空气法收集.
解答 解:(1)试管是常用的反应容器,水槽是常用的盛水的仪器,故答案为:试管;水槽;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;将制得的二氧化碳气体通入新制的澄清石灰水中,始终未出现浑浊现象,可能的原因是:二氧化碳中含有氯化氢气体;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;B;C;二氧化碳中含有氯化氢气体;
(3)如果用氯酸钾制氧气就需要加热,若用盛满水的F装置收集氧气,则氧气应从导管口b端进入,因为氧气的密度比水小;故答案为:A;b;
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,因此需要加热;常温下氨气(NH3)是一种无色、有刺激性气味、密度比空气小、极易溶于水的气体,因此只能用向下排空气法收集;故答案为:AD;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案| A. | 在量筒中进行化学反应 | |
| B. | 为了节约用剩的药品要放回原瓶 | |
| C. | 没说明用量时,固体药品取1~2克即可 | |
| D. | 给试管里的固体加热,管口要略向下 |
| A. | 浓硫酸放在空气中质量增加了 | B. | 爆炸 | ||
| C. | 烧碱溶液放在空气中质量增加了 | D. | 燃烧 |
| 选项 | 实验目的 | 实验方案 |
| A | 证明酸和碱恰好中和 | 向含有酚酞的氢氧化钠溶液中加入盐酸,溶液最终呈无色 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀硫酸,充分反应后,蒸发 |
| C | 确定放置在空气中的氢氧化钠固体的成分 | 取少量固体,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
| D | 鉴别氯化钠溶液,氢氧化钠溶液和稀盐酸 | 各取少量溶液于试管中,分别滴加紫色石蕊溶液,观察溶液颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 水是人类宝贵的资源 | B. | 水是由氢元素和氧元素组成的 | ||
| C. | 长期饮用蒸馏水有益健康 | D. | 自然界的水绝大多数都是混合物 |
| A. | 雪花飞舞 | B. | 鞭炮齐鸣 | C. | 冰雪消融 | D. | 波涛汹涌 |