题目内容
4.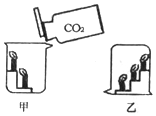 如图所示,甲烧杯中有高低两支燃烧的蜡烛,沿烧杯壁向烧杯中倾倒二氧化碳,乙图有三支高低燃烧的蜡烛,被罩在一只稍大一些的烧杯中,对甲、乙中蜡烛燃烧的现象描述正确的是( )
如图所示,甲烧杯中有高低两支燃烧的蜡烛,沿烧杯壁向烧杯中倾倒二氧化碳,乙图有三支高低燃烧的蜡烛,被罩在一只稍大一些的烧杯中,对甲、乙中蜡烛燃烧的现象描述正确的是( )| A. | 甲、乙都是自下而上依次熄灭 | |
| B. | 甲、乙都是自上而下依次熄灭 | |
| C. | 甲中自上而下依次熄灭,乙中自下而上依次熄灭 | |
| D. | 甲中自下而上依次熄灭,乙中自上而下依次熄灭 |
分析 甲烧杯中由于二氧化碳的密度比空气大,不燃烧、不支持燃烧,因此下层的蜡烛先熄灭.乙中中蜡烛燃烧产生二氧化碳气体,热的二氧化碳气体密度较小,二氧化碳上升后自上而下覆盖在烧杯中,二氧化碳不支持燃烧,因此高的蜡烛先熄灭,据此分析判断
解答 解:甲烧杯中由于二氧化碳的密度比空气大,不燃烧、不支持燃烧,因此下层的蜡烛先熄灭,上层的蜡烛后熄灭;乙中蜡烛燃烧产生二氧化碳气体,热的二氧化碳气体密度较小,二氧化碳上升后自上而下覆盖在烧杯中,二氧化碳不支持燃烧,因此高的蜡烛先熄灭,矮的蜡烛后熄灭.
由以上分析可知,D正确.
故选D.
点评 解答本题的关键是要掌握二氧化碳在不同情况下的性质,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
14.下列有关碳及其氧化物的说法错误的是( )
| A. | 金刚石、石墨和C60都是碳元素组成的单质,它们常温下性质稳定 | |
| B. | 金刚石、石墨的结构中碳原子的排列方式不同 | |
| C. | 木炭和一氧化碳都具有还原性,可用于冶炼金属 | |
| D. | CO2和CO都能与水反应,它们过多会增强温室效应 |
15.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明酸和碱恰好中和 | 向含有酚酞的氢氧化钠溶液中加入盐酸,溶液最终呈无色 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀硫酸,充分反应后,蒸发 |
| C | 确定放置在空气中的氢氧化钠固体的成分 | 取少量固体,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
| D | 鉴别氯化钠溶液,氢氧化钠溶液和稀盐酸 | 各取少量溶液于试管中,分别滴加紫色石蕊溶液,观察溶液颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质的用途中发生化学变化的是( )
| A. | 铁粉用于食品保存 | B. | 干冰用于人工降雨 | ||
| C. | 稀有气体用来制作电光源 | D. | 活性炭除冰箱中的异味 |
16.两份完全相同的稀盐酸分别与等质量的锌粉和镁粉反应,下列情况无法用所给的图象表示的是( )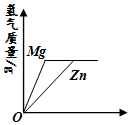

| A. | x轴表示加入稀盐酸的质量 | |
| B. | x轴表示反应时间 | |
| C. | x轴表示反应时间,Zn与稀盐酸恰好完全反应 | |
| D. | x轴表示加入金属质量 |
13.空气可被压缩说明( )
| A. | 分子由原子构成 | |
| B. | 加压时发生化学变化,产生更多氧气 | |
| C. | 分子体积很小 | |
| D. | 分子间有间隔 |
14.不规范的实验操作可能会影响化学实验的结果.下列实验操作中正确的是( )
| A. | 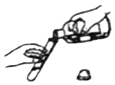 向试管中加入液体 | B. |  用胶头滴管吸取液体 | ||
| C. | 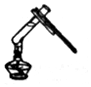 给盛有液体的试管加热 | D. | 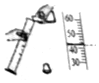 量取液体的值 |