题目内容
1.作为推行“低碳经济”的重要科技进步,太阳能光伏发电成为2010年上海世博会的“亮点”.太阳能光伏发电最关键的材料是高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法.生产流程示意如下: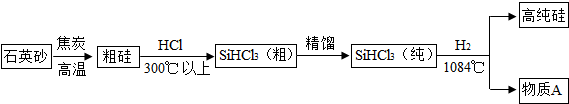
(1)石英砂的主要成分是SiO2,工业上制取粗硅的化学方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2R,R的化学式为CO;该反应的基本类型是置换反应.
(2)整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2,可能引起的后果是硅被氧化得不到高纯硅,还会引起爆炸.
(3)为了达到绿色化学和资源综合利用的目的,在生产过程中物质A需要循环使用,A的化学式是HCl.
分析 (1)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物R的化学式;由反应特征确定反应类型.
(2)根据混入O2,还原出的Si会被再次氧化,得不到高纯硅;可燃气体与空气或氧气混合达到爆炸极限,遇到明火,会发爆炸,进行分析解答.
(3)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
解答 解:(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2R,反应前硅、氧、碳原子个数分别为1、2、2,反应后的生成物中硅、氧、碳原子个数分别为1、0、0,根据反应前后原子种类、数目不变,则2R分子中含有2个碳原子和2个氧原子,则每个R分子由1个碳原子和1个氧原子构成,则物质X的化学式为CO.
该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(2)在H2还原SiHCl3过程中混入O2,还原出的Si会被再次氧化,得不到高纯硅;氢气具有可燃性,与氧气混合达到爆炸极限时在加热或点燃条件下会发生爆炸,故整个制备过程必须达到无水无氧.
(3)氢气与SiHCl3反应生成高纯硅和A(由质量守恒定律,反应前后元素种类不变,则该物质为氯化氢),该物质既是反应物,也是生成物,可以循环使用,A的化学式是HCl.
故答案为:(1)CO;置换反应;
(2)硅被氧化得不到高纯硅,还会引起爆炸;
(3)HCl.
点评 本题难度不大,理解生产高纯硅的流程图,掌握质量守恒定律、防止爆炸的措施等是正确解答本题的关键.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
12.下列四种物质,从组成上看有一种与其他三种明显不同的是( )
| A. | 水 | B. | 二氧化碳 | C. | 氧气 | D. | 过氧化氢 |
13.对下列四种粒子的结构示意图的理解,错误的是( )
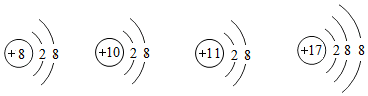
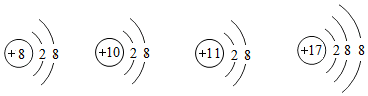
| A. | 它们都带电荷 | B. | 它们都具有相对稳定结构 | ||
| C. | 它们的核外电子排布不完全相同 | D. | 它们属于不同种元素 |
11.下列物质的用途主要有化学性质决定的是( )
| A. | 铜丝用于生产电线 | B. | 在实验室用浓硫酸做干燥剂 | ||
| C. | 葡萄糖给病人补充能量 | D. | 金刚石用来裁玻璃、切割大理石 |