题目内容
18.某工厂化验室用20%的氢氧化钠溶液来洗涤石油产品中的残余硫酸溶液490克,共消耗氢氧化钠溶液800克,洗涤后的溶液呈中性.试计算残余硫酸溶液中溶质的质量分数是多少?分析 根据溶质质量分数公式以及化学方程式进行计算,氢氧化钠能与硫酸反应生成硫酸钠和水,据此分析解答即可.
解答 解:所用氢氧化钠溶液中溶质的质量为800g×20%=160g;
设H2SO4的溶质质量分数为x
2NaOH+H2SO4=Na2SO4+2H2O
80 98
160g x×490g
$\frac{80}{160g}=\frac{98}{x×490g}$
x=40%
答案:残余硫酸溶液中溶质的质量分数是40%.
点评 此题是根据化学方程式计算的题目,解题的关键是根据已知量根据化学方程式对未知量进行的求解,属基础性计算考查题.

练习册系列答案
相关题目
8.下列物质中,属于纯净物的是( )
| A. | 三娘湾白酒 | B. | 雪碧饮料 | C. | 娃哈哈纯净水 | D. | 蒙牛酸奶 |
9.很多饮料中都含有柠檬酸(C6H8O7).下列关于柠檬酸的说法中正确的是( )
| A. | 属于氧化物 | |
| B. | 由6个碳原子、8个氢原子和7个氧原子组成 | |
| C. | 相对分子质量为192 | |
| D. | 分子中碳、氢、氧三种元素的质量比为6:8:7 |
6.以科学原理和实验事实为依据进行推理是学习化学的一种重要方法.下列推理得出的相关结论正确的是( )
| A. | 溶液是均一稳定的分散体系,所以均一稳定的分散体系一定是溶液 | |
| B. | 氢气与氧气混合点燃可能发生爆炸,所以点燃氢气前一定要检验氢气的纯度 | |
| C. | 盐酸与块状石灰石反应能制取CO2,所以稀硫酸也能与块状石灰石反应制取CO2 | |
| D. | 某物质在空气中燃烧生成CO2和H2O,所以该物质由C、H、O三种元素组成 |
13.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )


| A. | 20℃时,甲、乙的溶解度都是30克 | |
| B. | 40℃时,甲的溶解度小于乙的溶解度 | |
| C. | 升高温度能使乙的不饱和溶液变为饱和溶液 | |
| D. | 40℃时,甲的饱和溶液中溶质质量分数为50% |
10.化学与生活密切相关,下列说法不正确的是( )
| A. | 大量使用农药、化肥,提高农作物产量 | |
| B. | 回收利用废旧金属,有利于保护环境,充分利用资源 | |
| C. | 限制使用塑料袋,减少“白色污染” | |
| D. | 推广利用太阳能、风能,缓解“温室效应” |
7.为了测定一份铁镁混合粉末中铁的质量分数,某校化学兴趣小组取该样品8g分四次加入盛有100g未知浓度的硫酸溶液的烧杯(已知烧杯质量为50g)中,充分反应后,测得烧杯和烧杯内物质的质量数据记录如下:
(1)表中第三次加入混合粉末后,烧杯和烧杯内溶液的总质量是115.7g;
(2)所用硫酸溶液的溶质质量分数是14.7%;
(3)混合粉末中铁的质量分数是70%.
| 次数 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 2 | 2 | 2 | 2 |
| 烧杯和烧杯内物质的总质量/g | 151.9 | 153.8 | 157.7 |
(2)所用硫酸溶液的溶质质量分数是14.7%;
(3)混合粉末中铁的质量分数是70%.
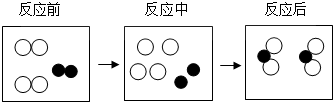
8.如图是某化学反应的微观模拟示意图( 表示一种原子,
表示一种原子, 表示另一种原子),从图中获得的有关信息不正确的是( )
表示另一种原子),从图中获得的有关信息不正确的是( )
 表示一种原子,
表示一种原子, 表示另一种原子),从图中获得的有关信息不正确的是( )
表示另一种原子),从图中获得的有关信息不正确的是( )
| A. | 化学反应中原子可以再分 | |
| B. | 化学反应中分子可以分为原子 | |
| C. | 化学反应中元素种类、原子种类和数目都没有改变 | |
| D. | 分子间存在一定的间隙 |
 科学就在我们身边.
科学就在我们身边.