题目内容
3.从古到今,人们对空气成分的研究一直都在进行.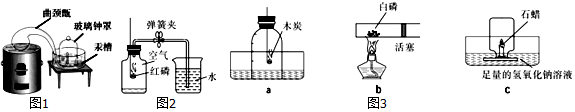
(1)二百多年前,法国化学家拉瓦锡用图1所示装置,定量测定了空气中氧气的含量,他把少量的汞放在密闭容器中加热12天.其目的是将容器内的氧气完全耗尽.其反应的化学方程式为2Hg+O2$\frac{\underline{\;\;△\;\;}}{\;}$2X,则X的化学式为HgO.
(2)目前,我们用图2所示装置来测定空气中氧气的含量,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,红磷燃烧的现象为
发出黄光、冒出白烟、放出热量.若操作不当.会产生实验误差.写出集气瓶内液面上升不足约$\frac{1}{5}$的一个原因是红磷的量不足(或装置的气密性不好或没有冷却至室温就打开止水夹).
(3)测定空气中氧气含量的装置还有很多,图3装置能达到实验目的是bc.
分析 (1)根据测定空气中氧气含量的要求以及质量守恒定律来分析;
(2)根据反应的原理书写化学方程式、根据磷燃烧的现象以及实验中国出现误差的原因来分析;
(3)根据反应后的产物来分析.
解答 解:(1)法国化学家拉瓦锡用图1所示装置,定量测定了空气中氧气的含量,他把少量的汞放在密闭容器中加热12天.其目的是将装置内的氧气完全耗尽,由质量守恒定律可知,反应前有:2个汞原子和2个氧原子,所以2X中含有2个汞原子和2个氧原子,所以X的化学式为HgO;故填:将容器内的氧气完全耗尽;HgO;
(2)磷与氧气在点燃的条件下反应生成五氧化二磷;红磷燃烧发出黄光、冒出白烟、放出热量;进行此实验时,必须保证装置的气密性良好,红磷足量,瓶子冷却后再打开弹簧夹,否则会导致结果不准确,故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;发出黄光、冒出白烟、放出热量;红磷的量不足(或装置的气密性不好或没有冷却至室温就打开止水夹);
(3)木炭燃烧后生成二氧化碳,装置内压强不变,无法测定空气中氧气的含量;白磷燃烧能消耗装置内的氧气,且生成物是固态,可测定出空气中氧气的含量;石蜡燃烧生成液态的水和二氧化碳气体,氢氧化钠溶液可以将二氧化碳完全吸收,所以该装置也可测定出空气中氧气的含量.故选bc.
点评 本题考查了空气中氧气含量的测定,掌握测定原理,药品的选择方法以及注意事项是解题的关键.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
13.下列各组溶液中不用其它试剂就无法鉴别出来的一组是( )
| A. | Na2CO3、BaCl2、NaCl、HCl | B. | CaCl2、NaCl、Na2CO3、BaCl2 | ||
| C. | NaOH、NaCl、HCl、石蕊 | D. | CuSO4、NaOH、Na2SO4、HCl |
14.科学探究一般包括“提出问题”“猜想与假设”“设计实验”“进行实验”“分析与论证”等几个环节.小明观察到建筑物的支柱一般为圆柱或四棱柱,他想了解支柱能承受的最大压力与支柱的形状是否有关,这一过程属于科学探究中哪一个环节( )
| A. | 提出问题 | B. | 设计实验 | C. | 进行实验 | D. | 分析与论证 |
8.如图是钾元素在元素周期表中的信息和钾原子的结构示意图.下列说法正确的是( )


| A. | 钾原子的核电荷数为19 | B. | 钾离子的符号为K+ | ||
| C. | 钾的相对原子质量为39.10g | D. | 化学反应中,钾原子易得电子 |
12.用图形“ ”、“
”、“ ”、“
”、“ ”分别表示质子数不同的原子,某反应过程的微观示意图为:
”分别表示质子数不同的原子,某反应过程的微观示意图为:

则可由此得出的正确结论是( )
 ”、“
”、“ ”、“
”、“ ”分别表示质子数不同的原子,某反应过程的微观示意图为:
”分别表示质子数不同的原子,某反应过程的微观示意图为:
则可由此得出的正确结论是( )
| A. | 图示中构成丙分子的原子数目最多 | B. | 反应前后三种原子的数目不变 | ||
| C. | 反应前后各物质的质量不变 | D. | 该反应一定属于置换反应 |
13.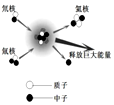 氘和氚是制造氢弹的原料.氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是( )
氘和氚是制造氢弹的原料.氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是( )
 氘和氚是制造氢弹的原料.氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是( )
氘和氚是制造氢弹的原料.氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是( )| A. | 氘和氚属于不同种元素 | |
| B. | 氘原子、氚原子和氦原子的中子数均相同 | |
| C. | 氘原子和氚原子的核电荷数分别为2,3 | |
| D. | 氚原子的原子核有1个质子和2个中子构成 |
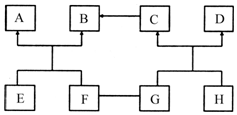
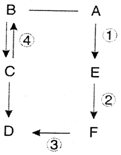 A、B、C、D、E、F都是初中化学中涉及的物质,已知A、B、C、D都是氧化物,且A是黑色固体,F是蓝色固体,相互间的转化关系如图(反应条件部分反应物、生成物略去),“-”表示连线两端的物质能发生反应,“→”表示一种物质能转化为另一种物质.回答:
A、B、C、D、E、F都是初中化学中涉及的物质,已知A、B、C、D都是氧化物,且A是黑色固体,F是蓝色固体,相互间的转化关系如图(反应条件部分反应物、生成物略去),“-”表示连线两端的物质能发生反应,“→”表示一种物质能转化为另一种物质.回答: