题目内容
8.如图是钾元素在元素周期表中的信息和钾原子的结构示意图.下列说法正确的是( )
| A. | 钾原子的核电荷数为19 | B. | 钾离子的符号为K+ | ||
| C. | 钾的相对原子质量为39.10g | D. | 化学反应中,钾原子易得电子 |
分析 A.根据原子结构示意图信息来分析;
B、根据离子符号的写法来分析;
C、根据图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,进行分析判断即可;
D、根据钾原子最外层电子数来分析.
解答 解:
A、由图示可知钾的原子序数为19,即核内有19个质子,质子数=核电荷数=19,故正确;
B、由结构示意图可知:钾原子最外层电子数为1,易失去1个电子,带1个单位的正电荷,符号为K+,故正确;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为39.10,相对原子质量单位是“1”,不是“克”,故错误;
D、由结构示意图可知:钾原子最外层电子数为1,易失去1个电子,故错误.
故选:AB.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
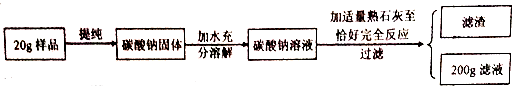
16.有一包白色粉末,其中可能含有BaCl2、CuSO4、NaCl、Na2CO3,为确定该白色粉末的成分,同学们进行了有关实验,实验流程和现象如下:
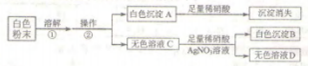
请回答以下问题.
(1)操作②的名称是过滤,①中发生反应的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
(2)通过以上实验可知,此白色粉末中一定含有BaCl2、Na2CO3;一定不含CuSO4,判断的理由是硫酸铜溶液显蓝色、BaCl2和Na2CO3反应产生碳酸钡沉淀.
(3)同学们利用下列两种方案继续对溶液D的成分进行检验,请选择一种方案进行回答.

请回答以下问题.
(1)操作②的名称是过滤,①中发生反应的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
(2)通过以上实验可知,此白色粉末中一定含有BaCl2、Na2CO3;一定不含CuSO4,判断的理由是硫酸铜溶液显蓝色、BaCl2和Na2CO3反应产生碳酸钡沉淀.
(3)同学们利用下列两种方案继续对溶液D的成分进行检验,请选择一种方案进行回答.
| 方案一 | 方案二 | |
| 操作 | 取少量溶液D,向其中滴加紫色石蕊溶液,观察到溶液变为红色 | 取少量溶液D,向其中滴加氢氧化钠溶液,无明显现象,再滴加碳酸钠溶液,观察到先有气泡产生,后产生白色沉淀 |
| 结论 | D中所含阳离子一定有 H+ | D中所含阳离子一定有 H+,Ba2+ |
17.保护环境人人有责.下列做法不符合这一理念的是( )
| A. | 按要求报废“黄标车” | B. | 随时随地焚烧处理垃圾 | ||
| C. | 合理使用风能发电 | D. | 用洗菜、淘米的水浇花、冲厕所 |
18.下列图象与叙述对应正确的是( )
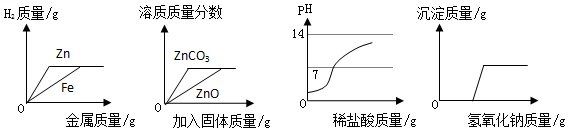

| A. | 将质量相等且足量的锌粉和铁粉分别投入相同质量、相同溶质质量分数的稀硫酸中 | |
| B. | 将一种稀硫酸均分成两份,分别向其中投入足量的氧化锌和碳酸锌 | |
| C. | 逐滴向一定量的氢氧化钠溶液中滴加稀盐酸直至过量 | |
| D. | 不断向稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 |
 摩拜、酷骑、OFO等共享自行车方便了人们的出行.
摩拜、酷骑、OFO等共享自行车方便了人们的出行.