题目内容
现有Cu和CuO的固体混合物20g,为了分析混合物中Cu和CuO的含量,小冰同学利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究.
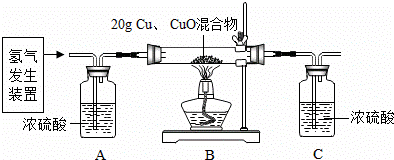
根据实验设计及有关数据进行分析与计算:
| 装置 | B | C |
| 反应前质量 | 85.3g | 284.2g |
| 反应后质量 | 82.1g | 287.8g |
(1)生成水的质量是 g.
(2)混合物中CuO的质量分数是为多少?(写出计算过程)
(3)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 (不用化简);
若玻璃管中的氧化铜没有完全反应,则求得水中氢、氧元素的质量比会 (选填“偏大”、“偏小”或“不变”).
答案 解:(1)浓硫酸具有吸水性,所以C装置增加的质量就是生成水的质量,所以生成水的质量是:287.8g﹣284.2g=3.6g;故答案为:3.6;
(2)设混合物中CuO的质量为x
CuO+H2 Cu+H2O
Cu+H2O
80 18
x 3.6g

x=16g
混合物中CuO的质量分数= =80%
=80%
答:混合物中CuO的质量分数为80%;
(3)根据B装置中减少的质量就是生成水中氧元素的质量,所以水中氢、氧元素的质量比=[(287.8g﹣284.2g)﹣(85.3g﹣82.1g)]:(85.3g﹣82.1g)];玻璃管中的氧化铜没有完全反应,则装置B中氧元素的质量就会减少,同时生成水的质量也减少,所以水中氢、氧元素的质量比会不变.故答案为:[(287.8g﹣284.2g)﹣(85.3g﹣82.1g)]:(85.3g﹣82.1g)];不变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 的化学方程式为
的化学方程式为 
 D.糖水
D.糖水 的“清洁绿色能源”专题展览引起各方关注。下列不属于绿色能源的是
的“清洁绿色能源”专题展览引起各方关注。下列不属于绿色能源的是