题目内容
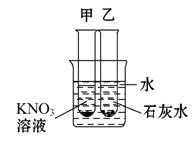
在生产生活中,你会发现“化学就在身边”。
(1)洗洁精能清除油污,这是利用它的________作用。
(2)上海世博园内安装的“直饮水”机,采用“活性炭+超滤层+紫外线”净水工艺。活性炭在此起_________作用,净化后的水属于________(选填
 “混合物”或“纯净物”)。
“混合物”或“纯净物”)。
(3)在农业生产中,施用的草木灰(有效成份为K2CO3)属于_______肥。在含有硫酸镁、硫酸铜的工业废水中加入过量的锌粉,充分反应后过滤,所得固体是(填写化学式)___________。
(4)化学对体育不仅雪中送炭,而且锦上添花。举重、体操等项目的运动员在比赛前常用白色的“镁粉”搓手,这是因为“镁粉”质轻、吸水性好,可做防滑剂。 “镁粉”的有效成份是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:
Mg5(OH)2(CO3)4 △ 5MgO+X+4CO2↑,则X的化学式是________;根据这些信息,还能推断出“镁粉”的另一种用途是________。
答案 (1)乳化 (2)吸附;混合物
(3)钾;Cu、Zn (4)H2O;干燥剂

现有Cu和CuO的固体混合物20g,为了分析混合物中Cu和CuO的含量,小冰同学利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究.
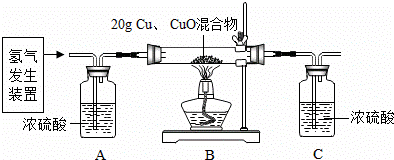
根据实验设计及有关数据进行分析与计算:
| 装置 | B | C |
| 反应前质量 | 85.3g | 284.2g |
| 反应后质量 | 82.1g | 287.8g |
(1)生成水的质量是 g.
(2)混合物中CuO的质量分数是为多少?(写出计算过程)
(3)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 (不用化简);
若玻璃管中的氧化铜没有完全反应,则求得水中氢、氧元素的质量比会 (选填“偏大”、“偏小”或“不变”).
溶解度可表示物质溶解性的大小。
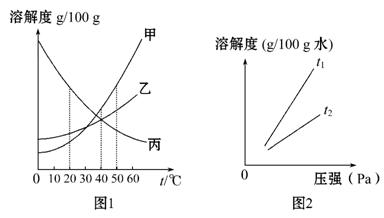
(1)如图1是甲、乙、丙三种固体 物质(均不含结晶水)的溶解度曲线。
物质(均不含结晶水)的溶解度曲线。
Ⅰ.40℃时,乙和丙 (填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅱ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃。请填表:
| 烧杯中的溶质 | 烧杯中固体的变化 |
| 甲 | |
| 乙 | 固体逐渐减少至全部溶解 |
| 丙 |
(2)Ⅰ.打开可乐瓶,逸出大量气体,由此可见,压强越小,CO2的溶解度越 ,若要加大二氧化碳溶解的量可采用的一种方法是 _______。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度 (填序号)。
a.大于40℃ b.小于40℃ c.无法确定
 2Fe+3CO2
2Fe+3CO2
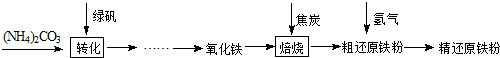
 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .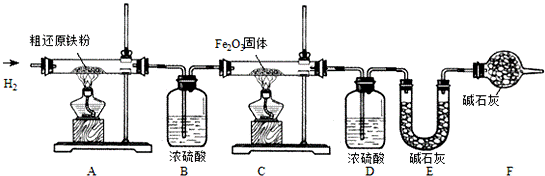
 3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).