题目内容
人体缺钙易产生“骨质疏松症”,补钙保健品“盖中盖”钙片中的有效成分为碳酸钙[CaCO3],试计算:
(1)碳酸钙的相对分子质量;
(2)碳酸钙中钙元素的质量分数;
(3)每片“盖中盖”钙片中含碳酸钙0.5g,成年人每天需要补钙0.4g,他应每天服用多少片“盖中盖”钙片?
答案 分析:
(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中元素的质量分数= ×100%,进行分析解答.
×100%,进行分析解答.
(3)根据题意,每片“盖中盖”钙片中含碳酸钙0.5g,成年人每天需要补钙0.4g,由化合物中某元素的质量=该化合物的质量×该元素的质量分数进行分析解答.
解:(1)碳酸钙的相对分子质量是40+12+16×3=100.
(2)碳酸钙中钙元素的质量分数为 100%=40%.
100%=40%.
(3)根据题意,每片“盖中盖”钙片中含碳酸钙0.5g,则含碳元素的质量为0.5g×40%=0.2g;成年人每天需要补钙0.4g,他应每天服用“盖中盖”钙片的片数为0.4g÷0.2g=2片.
故答案为:(1)100;(2)40%;(3)2.

 全优点练单元计划系列答案
全优点练单元计划系列答案现有Cu和CuO的固体混合物20g,为了分析混合物中Cu和CuO的含量,小冰同学利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究.
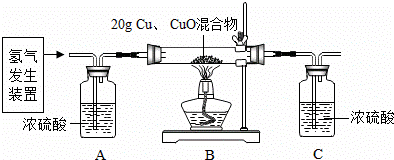
根据实验设计及有关数据进行分析与计算:
| 装置 | B | C |
| 反应前质量 | 85.3g | 284.2g |
| 反应后质量 | 82.1g | 287.8g |
(1)生成水的质量是 g.
(2)混合物中CuO的质量分数是为多少?(写出计算过程)
(3)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 (不用化简);
若玻璃管中的氧化铜没有完全反应,则求得水中氢、氧元素的质量比会 (选填“偏大”、“偏小”或“不变”).
学习中我们接触过胆矾,(化学式为CuSO4·5H2O),胆矾的相对分子质量为250。
(1)请你分析出胆矾相对分子质量的计算方法,并用该方法算出FeSO4·7H2O
的相对分子质量。
(2)铁是人类生命活动不可缺少的微量元素,正常人每天补充14mg左右的铁,其中大部分来自食物。如果全部通过服用含FeSO4·7H2O的片剂补充铁,计算每天约需要服用含FeSO4·7H2O片剂的质量。
| 温馨提示 胆矾(CuSO4·5H2O)的相对分子质量=64+(32+4×16)+5(2+16) |

 入少量植物油并点燃,小明用坩埚钳把小铁盒放在冰水共存的液面上,观察到火焰立即熄灭,该实验证明了灭火的原理是______________________________,小刚同学将一块湿抹布盖在小铁盒上,火焰也立即熄灭,他依据的灭火原理是_______________
入少量植物油并点燃,小明用坩埚钳把小铁盒放在冰水共存的液面上,观察到火焰立即熄灭,该实验证明了灭火的原理是______________________________,小刚同学将一块湿抹布盖在小铁盒上,火焰也立即熄灭,他依据的灭火原理是_______________ 么?质量分别是多少克?(3)原混合物中氯酸钾的百分含量是多少?(保留一位小数)
么?质量分别是多少克?(3)原混合物中氯酸钾的百分含量是多少?(保留一位小数)
 和
和 化学性质相似
化学性质相似  是保持氧气化学性质的微粒
是保持氧气化学性质的微粒
 出电源正负极。
出电源正负极。
 。
。