题目内容
11.下图所示实验装置或实验操作正确的是( )| A. |  除去CO中少量的CO2 | B. |  检查装置的气密性 | ||
| C. |  加热蒸发NaCl溶液 | D. |  稀释浓H2SO4 |
分析 A、根据二氧化碳能与氢氧化钠溶液反应,一氧化碳不与氢氧化钠溶液反应,进行分析判断.
B、装置气密性检验的原理是:通过气体发生器与液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏.
C、根据蒸发操作的注意事项进行分析判断.
D、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
解答 解:A、二氧化碳能与氢氧化钠溶液反应,一氧化碳不与氢氧化钠溶液反应,除去CO中少量的CO2可选用氢氧化钠溶液,图中装置起洗气功能时进气管与出气管的方向是“长进短出”,图中进气管与出气管的方向错误,图中所示操作错误.
B、该选项用的是空气热胀冷缩法,原理为:关闭弹簧夹,用手掌紧握烧瓶外壁,若玻璃管内产生一段水柱,则证明气密性良好,图中所示操作正确.
C、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,图中没有用玻璃棒搅拌,所示操作错误.
D、稀释浓硫酸时,要把浓硫酸缓缓地沿烧杯壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;不能在量筒内稀释浓硫酸,图中所示操作错误.
故选:B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
2.下列不发生化学变化的是( )
| A. |  我国古代烧制陶器 | B. | 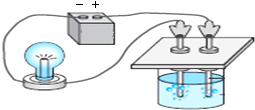 测定酸碱盐溶液导电性 | ||
| C. | 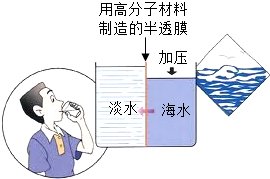 用高分子分离膜淡化海水 | D. |  二氧化碳作气体肥料 |
19.“五水共治,治污为先”是我省提出改善生态环境的一项重要政策.为了防止水体污染,你认为下列措施中可行的是( )
| A. | 任意排放工业污水 | B. | 禁止使用农药和化肥 | ||
| C. | 生活污水经净化处理后再排放 | D. | 医院污水直接排放到河流中 |
3.德国化学家格哈德•埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )


| A. | 此反应有化合物参加 | |
| B. | 原子在化学变化中是可分的 | |
| C. | 符合上述反应过程的顺序是③①② | |
| D. | 对应化学反应方程式为2N+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 |
20. 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
【提出猜想】红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】
(1)白色无水CuSO4遇水变蓝
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu2FeCl2+CuCl2
【实验探究】
[甲组同学]:定性检测该红色粉末的物质组成
(1)小云取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想①(填序号)一定不成立.
(2)小伟向小云得到的有色溶液中插多余空入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色固体出现,得出猜想③(填序号)成立.
[乙组同学]:定量测定该红色粉末中氧化铁的质量分数
实验步骤:小晨称取该红色粉末5.0g装入硬质玻璃管中,按右图进行实验.开始时缓缓通入CO气体,过一段时间后再高温加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如表:
【交流讨论】
(1)在装置A中先通CO气体的目的是排出玻璃管内的空气,B装置的作用是吸收反应产生的CO2.
(2)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
(3)从环保角度看上述装置有严重不足之处.你认为应该如何改进?管口放置点燃的蜡烛或气囊收集.
【拓展延伸】
对实验后B装置洗气瓶内溶液做进一步探究
实验步骤:小渊同学取该洗气瓶内溶液50克,逐滴加入氢氧化钙溶液至无沉淀析出,共得沉淀5克.试计算:洗气瓶内的溶液中碳酸钠的质量分数.
 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.【提出猜想】红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】
(1)白色无水CuSO4遇水变蓝
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu2FeCl2+CuCl2
【实验探究】
[甲组同学]:定性检测该红色粉末的物质组成
(1)小云取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想①(填序号)一定不成立.
(2)小伟向小云得到的有色溶液中插多余空入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色固体出现,得出猜想③(填序号)成立.
[乙组同学]:定量测定该红色粉末中氧化铁的质量分数
实验步骤:小晨称取该红色粉末5.0g装入硬质玻璃管中,按右图进行实验.开始时缓缓通入CO气体,过一段时间后再高温加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如表:
| 反应前 | 反应后 | ||
| Ⅰ组 | 玻璃管和红色粉末的总质量 | 48.3克 | 47.1克 |
| Ⅱ组 | 洗气瓶和瓶中所盛物质的总质量 | 258.6克 | 261.9克 |
(1)在装置A中先通CO气体的目的是排出玻璃管内的空气,B装置的作用是吸收反应产生的CO2.
(2)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
(3)从环保角度看上述装置有严重不足之处.你认为应该如何改进?管口放置点燃的蜡烛或气囊收集.
【拓展延伸】
对实验后B装置洗气瓶内溶液做进一步探究
实验步骤:小渊同学取该洗气瓶内溶液50克,逐滴加入氢氧化钙溶液至无沉淀析出,共得沉淀5克.试计算:洗气瓶内的溶液中碳酸钠的质量分数.
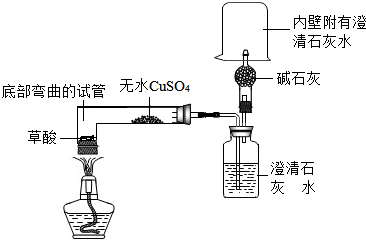 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究: 为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:取20g固体样品,全部溶于100g水中,向所得的混合溶液中滴加碳酸钠溶液,记录并绘制了如图所示的曲线.
为测定由氯化钙和氯化钠组成的固体样品中氯化钙的含量,某同学进行了如下实验:取20g固体样品,全部溶于100g水中,向所得的混合溶液中滴加碳酸钠溶液,记录并绘制了如图所示的曲线.