题目内容
4.已知浓硫酸可与Zn反应生成SO2,其反应方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O.下列有关叙述中,正确的是( )| A. | 浓硫酸能电离出氢离子,但不具有酸的通性 | |
| B. | 将足量的Zn放入少量的浓硫酸中,反应后生成的气体只有SO2 | |
| C. | 在上述化学反应中,反应物之间电子发生了转移,属于氧化还原反应 | |
| D. | 在上述化学反应前后,溶液的质量相等,遵循质量守恒定律 |
分析 A、浓硫酸能电离出氢离子,具有酸的通性;
B、当锌与浓硫酸反应时,随着浓硫酸的不断消耗,浓硫酸逐渐变成稀硫酸,锌能与稀硫酸反应生成氢气;
C、有电子发生转移的反应,属于氧化还原反应;
D、上述化学反应前后,溶液的质量减少.
解答 解:A、浓硫酸能电离出氢离子,具有酸的通性,错误;
B、当锌与浓硫酸反应时,随着浓硫酸的不断消耗,浓硫酸逐渐变成稀硫酸,锌能与稀硫酸反应生成氢气,故反应后生成的气体有SO2和氢气,错误;
C、在上述化学反应中,反应物之间电子发生了转移,属于氧化还原反应,正确;
D、上述化学反应前后,溶液的质量减少,错误.
故选C.
点评 本题考查了金属的性质和酸的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.将汽车尾气中的有毒气体转化为空气中的成分,其微观结构示意图如下,说法不严谨的是( )
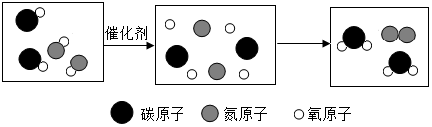

| A. | 反应前有两种物质的分子 | |
| B. | 化学变化的本质是:分子分成原子,原子重新组合成新物质的分子 | |
| C. | 在化学变化中,分子分成原子,原子重新组合成新物质 | |
| D. | 图中共有三种氧化物 |
15.下列图示实验操作中,不正确的是( )
| A. |  过滤 | B. |  滴加液体 | ||
| C. |  加热液体 | D. |  检查装置的气密性 |
12.为得知7克高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
请回答:
(1)在本实验条件下氧气的密度为1.4×10-3克/厘米3,则由小柯的测量结果可以算出7克高锰酸钾分解后所产生的氧气质量为0.84克;
(2)大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是B;
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请通过化学方程式计算7克高锰酸钾完全分解所产生的氧气质量;
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:可能是生成锰酸钾或二氧化锰分解放出了氧气.
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师指导下,将7克高锰酸钾充分加热,得到氧气600厘米3 | 解:高锰酸钾中氧元素的质量分数: =$\frac{O的相对原子质量×4}{KMn{O}_{4}的相对分子质量}$×100%=$\frac{16×4}{39+55+16×4}$×100%=40.5% 氧气的质量为7克×40.5%=2.84克 答:7克高锰酸钾完全分解产生氧气2.84克. |
(1)在本实验条件下氧气的密度为1.4×10-3克/厘米3,则由小柯的测量结果可以算出7克高锰酸钾分解后所产生的氧气质量为0.84克;
(2)大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是B;
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请通过化学方程式计算7克高锰酸钾完全分解所产生的氧气质量;
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:可能是生成锰酸钾或二氧化锰分解放出了氧气.
13.下列各组物质能在pH=1的无色溶液中大量共存的是( )
| A. | ZnSO4 NaNO3 KCl | B. | Cu(NO3)2 NaCl KNO3 | ||
| C. | Na2CO3 KNO3 NH4Cl | D. | K2SO4 Ba(OH)2 KCl |
14.金属冶炼就是要把金属从化合态变成游离态,使金属氧化物还原成金属单质,如图为有关实验室用一氧化碳还原氧化铜的实验装置,装置乙中的溶液为澄清石灰水,请回答与该实验有关的问题:

(1)实验时,从甲装置的玻璃管中观察到
的现象是黑色固体变成红色
(2)装置乙中发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O
(3)现有含杂质的氧化铜样品10g(假设杂质不参加反应),为测定该样品中氧化铜的质量分数,某同学用如图所示的装置进行实验,得到下列两组数据:
关于这两组数据,下列说法不正确的是BD(选填相关的字母)
A、玻璃管中固体减少的质量即为氧化铜中氧元素的质量
B、利用这两个数据都可以计算出样品中氧化铜的质量分数
C、装置乙中石灰水增重的质量与反应产生二氧化碳的质量不相等
D、如果实验称量很准确,则玻璃管中固体减少的质量应等于装置乙中石灰水增重的质量
(4)通过计算该样品中氧化铜的质量分数为90%.

(1)实验时,从甲装置的玻璃管中观察到
的现象是黑色固体变成红色
(2)装置乙中发生反应的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O
(3)现有含杂质的氧化铜样品10g(假设杂质不参加反应),为测定该样品中氧化铜的质量分数,某同学用如图所示的装置进行实验,得到下列两组数据:
| 反应前 | 氧化铜完全反应后 | |
| Ⅰ组 | 洗气瓶和石灰水的质量为185g | 洗气瓶和瓶内物质的总质量为187g |
| Ⅱ组 | 玻璃管和氧化铜样品的质量为57.9g | 玻璃管和玻璃管内物质的质量为56.1g |
A、玻璃管中固体减少的质量即为氧化铜中氧元素的质量
B、利用这两个数据都可以计算出样品中氧化铜的质量分数
C、装置乙中石灰水增重的质量与反应产生二氧化碳的质量不相等
D、如果实验称量很准确,则玻璃管中固体减少的质量应等于装置乙中石灰水增重的质量
(4)通过计算该样品中氧化铜的质量分数为90%.