题目内容
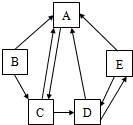 A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):
A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):(1)A为
(2)A和B反应是
(3)写化学方程式:C→D:
考点:物质的鉴别、推断,化学式的书写及意义,物质发生化学变化时的能量变化,书写化学方程式、文字表达式、电离方程式
专题:框图型推断题
分析:根据A、B、C、D、E是初中化学常见五种化合物,A、B、E都是氧化物,且B和E能够转化成A,所以A是水,所以B、E是金属氧化物或非金属氧化物,B、C、D都含有相同的阳离子,所以B是金属氧化物,E是非金属氧化物,结合框图的转化关系,猜想B可能是氧化钙,C是氢氧化钙,D是碳酸钙,E是二氧化碳,然后将猜想的物质代入转化关系中验证即可.
解答:解:(1)A、B、C、D、E是初中化学常见五种化合物,A、B、E都是氧化物,且B、E能够转化成A,所以A是水,所以B和E是金属氧化物或非金属氧化物,B、C、D都含有相同的阳离子,所以B是金属氧化物,E是非金属氧化物,结合框图的转化关系,猜想B可能是氧化钙,C是氢氧化钙,D是碳酸钙,E是二氧化碳,氧化钙和盐酸会生成水,二氧化碳和氢氧化钙会生成水,氧化钙和水会生成氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙,碳酸钙高温会生成二氧化碳,氢氧化钙和盐酸会生成水,碳酸钙和盐酸也会生成水,推出的各种物质均满足题意,推导合理,所以A是H2O,B是CaO,D是CaCO3;
(2)通过推导可知,A是水,B是氧化钙,氧化钙和水会生成氢氧化钙,放出大量的热,所以该反应是放热反应;
(3)C→D是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
B→A是氧化钙和盐酸反应生成氯化钙和水,化学方程式为:CaO+2HCl=CaCl2+H2O.
故答案为:(1)H2O,CaO,CaCO3;
(2)放热;
(3)Ca(OH)2+CO2=CaCO3↓+H2O;
CaO+2HCl=CaCl2+H2O.
(2)通过推导可知,A是水,B是氧化钙,氧化钙和水会生成氢氧化钙,放出大量的热,所以该反应是放热反应;
(3)C→D是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
B→A是氧化钙和盐酸反应生成氯化钙和水,化学方程式为:CaO+2HCl=CaCl2+H2O.
故答案为:(1)H2O,CaO,CaCO3;
(2)放热;
(3)Ca(OH)2+CO2=CaCO3↓+H2O;
CaO+2HCl=CaCl2+H2O.
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
 两个同学做了一个有趣的实验,装置如图.
两个同学做了一个有趣的实验,装置如图.



 如图表示的是电解水反应的微观示意图,回答下列问题:
如图表示的是电解水反应的微观示意图,回答下列问题: