题目内容
有一气体混合物含有二氧化碳、一氧化碳、氮气和水蒸气四种气体,现进行如下操作,请回答:(假设每步反应都进行完全)
(1)依次通过NaOH溶液、浓硫酸,此过程中发生反应的化学方程式为 ;
(2)依次通过浓硫酸、炽热的氧化铁粉末,最后得到的气体有 (填化学式)
(1)依次通过NaOH溶液、浓硫酸,此过程中发生反应的化学方程式为
(2)依次通过浓硫酸、炽热的氧化铁粉末,最后得到的气体有
考点:气体的净化(除杂),书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯,物质的分离、除杂、提纯与共存问题
分析:混合气体通过每一步时会有一些气体会发生化学反应并被除去,有时气体会被彻底除去,有时除去一种气体的同时又会生成另一种气体;二氧化碳能与NaOH溶液反应,一氧化碳能与炽热的氧化铁粉末反应,浓硫酸具有吸水性,据此结合题意进行分析解答可.
解答:解:(1)有一气体混合物含有二氧化碳、一氧化碳、氮气和水蒸气四种气体,通过NaOH溶液,二氧化碳会与NaOH溶液反应生成碳酸钠和水,CO2被吸收;再通过浓硫酸除去水蒸气;此过程中发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O;
(2)浓硫酸具有吸水性,通过浓硫酸,能除去水蒸气;通过炽热的氧化铁粉末,一氧化碳与氧化铁反应生成铁和二氧化碳,一氧化碳被吸收;最后剩余的气体为N2、CO2.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;(2)N2、CO2.
(2)浓硫酸具有吸水性,通过浓硫酸,能除去水蒸气;通过炽热的氧化铁粉末,一氧化碳与氧化铁反应生成铁和二氧化碳,一氧化碳被吸收;最后剩余的气体为N2、CO2.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;(2)N2、CO2.
点评:本题难度不大,熟练掌握常见气体的性质是正确解答此类题的关键;解题时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
人类生活需要能量,下列能量主要由化学变化产生的是( )
| A、液化石油气燃烧放出的热量 |
| B、电灯通电发出的光 |
| C、水电站利用水力产生的电能 |
| D、电熨斗通电发出的热量 |
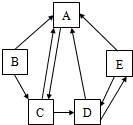 A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):
A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):

 生产、生活中常需配制溶液.
生产、生活中常需配制溶液.