题目内容
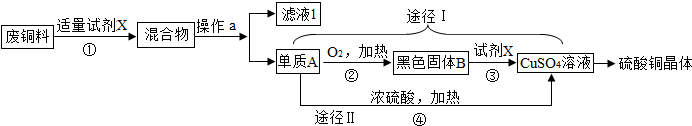
根据下列实验装置图,回答有关问题,

(1)图中标有①的仪器名称是 .
(2)实验室制取氢气应选择的发生装置为 (填字母),若要获得较纯净的氢气,应选择的收集装置是 (填字母).为保证安全,点燃氢气前,应进行的操作是 .
(3)实验室利用过氧化氢溶液和二氧化锰制氧气,反应的化学方程式为 .若用B装置作制氧气的发生装置,应进行的改进是 .
(4)人教版高中教材《化学1》显示,过氧化钠(Na2O2)和二氧化碳反应生成碳酸钠和氧气,化学方程式为
2Na2O2+2CO2═2Na2CO3+O2.小翔同学和小何同学分别设计了图甲和图乙的实验装置,检查气密性良好后进行实验验证.预热后对试管进行加热(2NaHCO3
Na2CO3+CO2↑+H2O).观察到图甲浓硫酸中有气泡产生,蚊香熄灭.浓硫酸的作用是 .观察图乙中的现象是 ,说明有氧气产生.由资料和实验可得出的结论是 .


(1)图中标有①的仪器名称是
(2)实验室制取氢气应选择的发生装置为
(3)实验室利用过氧化氢溶液和二氧化锰制氧气,反应的化学方程式为
(4)人教版高中教材《化学1》显示,过氧化钠(Na2O2)和二氧化碳反应生成碳酸钠和氧气,化学方程式为
2Na2O2+2CO2═2Na2CO3+O2.小翔同学和小何同学分别设计了图甲和图乙的实验装置,检查气密性良好后进行实验验证.预热后对试管进行加热(2NaHCO3
| ||

考点:常用气体的发生装置和收集装置与选取方法,气体的净化(除杂),实验室制取氧气的反应原理,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途和使用方法;
(2)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(4)浓硫酸具有吸水性,可以用来干燥二氧化碳,氧气能够支持燃烧.
(2)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(4)浓硫酸具有吸水性,可以用来干燥二氧化碳,氧气能够支持燃烧.
解答:解:(1)标有①的仪器名称是集气瓶,常用来收集气体.
故填:集气瓶.
(2)实验室制取氢气不需要加热,应选择的发生装置为A装置;氢气的密度比空气小,可以用向下排空气法收集,即用E装置收集,氢气不溶于水,可以用排水法收集,即用C装置收集,利用排水法收集的氢气比较纯净;
氢气与空气或氧气混合达到爆炸极限时,遇明火会发生爆炸,为保证安全,点燃氢气前,应进行的操作是验纯.
故填:A;C;验纯.
(3)实验室利用过氧化氢溶液和二氧化锰制氧气,反应的化学方程式为:2H2O2
2H2O+O2↑;
若用B装置作制氧气的发生装置,应进行的改进是在试管口塞一团棉花.
故填:2H2O2
2H2O+O2↑;在试管口塞一团棉花.
(4)浓硫酸的作用是干燥二氧化碳;
观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,即过氧化钠和二氧化碳反应生成了氧气;
甲中和过氧化钠混合的二氧化碳是干燥的,不容易和过氧化钠反应,因此没有反应的二氧化碳能使燃烧的蚊香熄灭,而乙中的二氧化碳中含有水蒸气,容易和过氧化钠反应生成氧气,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应.
故填:干燥二氧化碳;蚊香燃烧更剧烈;湿润的二氧化碳更容易和过氧化钠反应.
故填:集气瓶.
(2)实验室制取氢气不需要加热,应选择的发生装置为A装置;氢气的密度比空气小,可以用向下排空气法收集,即用E装置收集,氢气不溶于水,可以用排水法收集,即用C装置收集,利用排水法收集的氢气比较纯净;
氢气与空气或氧气混合达到爆炸极限时,遇明火会发生爆炸,为保证安全,点燃氢气前,应进行的操作是验纯.
故填:A;C;验纯.
(3)实验室利用过氧化氢溶液和二氧化锰制氧气,反应的化学方程式为:2H2O2
| ||
若用B装置作制氧气的发生装置,应进行的改进是在试管口塞一团棉花.
故填:2H2O2
| ||
(4)浓硫酸的作用是干燥二氧化碳;
观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,即过氧化钠和二氧化碳反应生成了氧气;
甲中和过氧化钠混合的二氧化碳是干燥的,不容易和过氧化钠反应,因此没有反应的二氧化碳能使燃烧的蚊香熄灭,而乙中的二氧化碳中含有水蒸气,容易和过氧化钠反应生成氧气,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应.
故填:干燥二氧化碳;蚊香燃烧更剧烈;湿润的二氧化碳更容易和过氧化钠反应.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
 A、B、C、D、E、F是初中化学中常见的七种物质,它们之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体且组成元素相同,E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是:
A、B、C、D、E、F是初中化学中常见的七种物质,它们之间的相互转化关系如图所示.已知常温下B、C为气体,且B是植物进行光合作用的一种重要原料;D、F均为无色液体且组成元素相同,E为黑色固体,与稀硫酸反应得到蓝色溶液(部分反应物和生成物及反应条件已略去).下列有关判断正确的是:
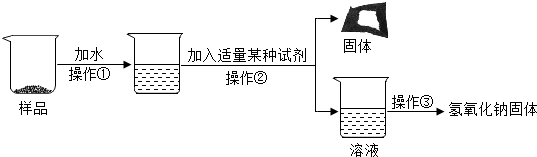
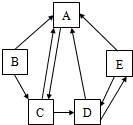 A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):
A、B、C、D、E是初中化学常见五种化合物,其中A、B、E都是氧化物,B、C、D都含有相同阳离子,它们转化如图所示(图中“→”间存在转化关系:图中已略去部分物质):