题目内容
6.小明要用100g质量分数为10%的NaOH溶夜老制作叶脉书签.如图是配制氢氧化钠溶液的实验操作示意图
(1)称量强氧化钠固体10g,量筒取水90mL,
(2)量取水应选择100mL(填10mL,50mL,100mL)的量筒
(3)指出图中的一处操作错误:视线要与凹液面的最低处保持水平进
(4)用上述图示的序号表示配制溶液的操作顺序:④①③⑤②
(5)反思:所配制的溶液质量分数会偏小(填偏大或偏小或影响)
(6)?中使用玻璃棒的作用:搅拌,加速溶解.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量.
(2)根据所量取水的体积确定所用量筒的量程.
(3)根据托盘天平的使用要遵循“左物右码”的原则、量筒读数时视线要与凹液面的最低处保持水平进行分析解答.
(4)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(5)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,100g质量分数为10%的氢氧化钠溶液,需氢氧化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需蒸馏水的质量=100g-10g=90g
(2)水的密度为1g/cm3,则根据V=$\frac{m}{ρ}$=$\frac{90g}{1g/c{m}^{3}}$=90cm3=90mL,应选用100mL的量筒.
(3)托盘天平的使用要遵循“左物右码”的原则,图①中氢氧化钠与砝码的位置颠倒.
量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度,操作错误.
(4)配制100g质量分数为10%的氢氧化钠溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,用图示的序号表示为:④①③⑤②.
(5)量取液体时,仰视刻度,水偏多,则所配制的溶液质量分数会偏小;
(6)试验中玻璃棒的作用:搅拌,加速溶解.
故答案为:
(1)10;90;(2)100;(3)图①中氢氧化钠与砝码的位置颠倒;量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度等;
(4)④①③⑤②;(5)偏小;(6)搅拌,加速溶解..
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、溶液稀释前后溶质的质量不变等是正确解答本题的关键.

 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案| A. | 1% | B. | 90% | C. | 10% | D. | 11.1% |
| A. | 镁条燃烧发出耀眼的强光,生成白色的氧化镁 | |
| B. | 红磷在氧气中剧烈燃烧,产生大量的白雾 | |
| C. | 硫在空气中燃烧产生淡蓝色火焰 | |
| D. | 水电解时生成的氧气和氢气的体积比约为1:2 |
| A. | 二氧化硫、二氧化氮、二氧化碳 | B. | 二氧化硫、二氧化氮、一氧化碳 | ||
| C. | 二氧化硫、一氧化碳、氢气 | D. | 二氧化氮、一氧化碳、水蒸气 |
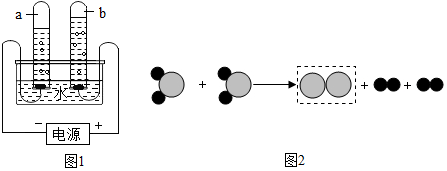
 ”表示两种不同原子.该反应属于分解(填基本反应类型)反应.
”表示两种不同原子.该反应属于分解(填基本反应类型)反应.
