题目内容
12.关于 CaCO3的说法正确的是( )| A. | 由钙、碳、氧三个元素组成 | B. | 碳元素的化合价为+2 | ||
| C. | 钙元素的质量分数为40% | D. | 属于氧化物 |
分析 A.根据元素的规定来分析;
B.根据化合物中元素化合价的计算方法来分析;
C.根据化合物中元素质量分数的计算方法来分析;
D.根据氧化物的概念来分析.
解答 解:A.碳酸钙是由碳、氢、氧三种元素组成的,元素是个宏观概念,只讲种类、不讲个数,故错误;
B.碳酸钙中,钙元素显+2价,氧元素显-2价,设其中钙元素的化合价为x,则(+2)+x+(-2)×3=+4,故错误;
C.碳酸钙中,钙元素的质量分数为:$\frac{40}{40+12+16×3}×100%$=40%,故正确;
D.氧化物是由两种元素组成的,而碳酸钙中含有三种元素,故错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
7.如图为A,B,C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
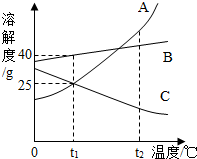

| A. | t2℃时,三种物质的饱和溶液中A溶液的溶质质量分数最大 | |
| B. | t1℃时,三种物质的溶解度由大到小的顺序为:B>A=C | |
| C. | 要将C的接近饱和的溶液转化为饱和溶液可以采用升温的方法 | |
| D. | A中混有少量B,可采用冷却热饱和溶液的方法提纯A |
4.下列实验操作中,正确的是( )
| A. | 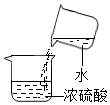 稀释浓硫酸 | B. | 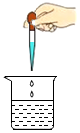 滴加液体 | C. | 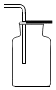 收集气体 | D. | 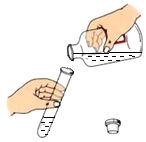 倾倒液体药品 |
1.下列说法正确的是( )
| A. | 将不饱和溶液变为饱和溶液不能采用升高温度的方法 | |
| B. | 将10g食盐溶解在100g水中,所得溶液的溶质质量分数为10% | |
| C. | 将100g饱和的食盐溶液中取出的5g,则变为不饱和溶液 | |
| D. | 当溶液被水稀释时,溶液中保持不变的是溶质的质量 |
2. 化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.
化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.
【猜想与假设】
(1)没有反应,溶液为NaOH溶液
(2)发生反应,溶液为Na2CO3溶液
(3)发生反应,溶液为Na2CO3和NaOH的混合溶液
【设计实验】
【实验结论】对于现象不明显的化学反应可以通过加入指示剂来判断反应是否发生.
【结论与反思】通过该探究,氢氧化钠溶液应密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:胶头滴管中吸入某种液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的体积的影响).完成下列表格:
 化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.
化学课上,老师将CO2分别通入澄清石灰水和氢氧化钠溶液中,我们观察到前者变浑浊,后者没有明显现象,CO2和NaOH是否发生了化学反应呢?同学们对反应后的溶液进行探究.【猜想与假设】
(1)没有反应,溶液为NaOH溶液
(2)发生反应,溶液为Na2CO3溶液
(3)发生反应,溶液为Na2CO3和NaOH的混合溶液
【设计实验】
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 取反应后的溶液少许于试管 中,向试管中滴加几滴酚酞试液,振荡 | 若溶液变红,则猜想(2)(3)不成立 | 同学认为:此方案结论不正确,理由是碳酸钠溶液能使酚酞试液变红色. |
| 第2组 | 取反应后的溶液少许于试管中,向试管中加入足量的CaCl2(呈中性)溶液,振荡. | 若产生白色沉淀,反应方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl,则猜想(1)不成立. | 猜想(2)(3)尚无法确定其一. |
| 第3组 | 将第2组实验后的混合物过滤,向滤液中滴加氯化铜溶液 | 若无蓝色沉淀,则猜想(2)成立,若有蓝色沉淀,则猜想(3)成立. | 也可以用酚酞试液(填试剂名称)也能达到实验目的. |
【结论与反思】通过该探究,氢氧化钠溶液应密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:胶头滴管中吸入某种液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的体积的影响).完成下列表格:
| 符合装置乙实验现象的试剂组合为 | 胶头滴管内液体 | 瓶中物质 | |
| 1 | NaOH溶液或水 | CO2 | |
| 2 | 石灰水 | CO2 | |
| 3 | 水 | 氨气 | |
| 4 | NaOH溶液 | 氯化氢 | |
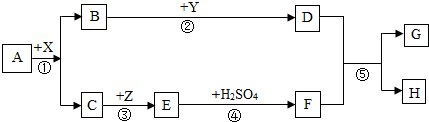
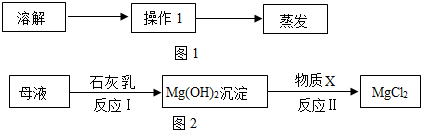
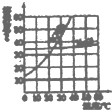 根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.
根据如图KNO3和 NaCl两种由体物质的溶解度曲线.回答下列问题.