题目内容
7.如图为A,B,C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )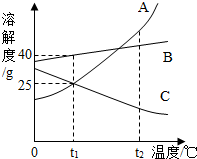
| A. | t2℃时,三种物质的饱和溶液中A溶液的溶质质量分数最大 | |
| B. | t1℃时,三种物质的溶解度由大到小的顺序为:B>A=C | |
| C. | 要将C的接近饱和的溶液转化为饱和溶液可以采用升温的方法 | |
| D. | A中混有少量B,可采用冷却热饱和溶液的方法提纯A |
分析 A、据该物质下物质的溶解度及饱和溶液中溶质的质量分数分析解答;
B、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
C、C的溶解度随温度升高而减小,所以其不饱和溶液变为饱和溶液可采取升温的方法;
D、A的溶解度随温度升高而增大,B的溶解度受温度影响不大,所以A中混有少量B,可采用蒸发结晶的方法提纯B.
解答 解:A、t2℃时,三种物质的溶解度大小顺序是:A>B>C;由饱和溶液中溶质的质量分数计算式$\frac{溶解度}{溶解度+100g}$×100%可知:溶解度越大则饱和溶液中溶质的质量分数越大,故此时饱和溶液质量分数最大的是A,正确;
B、t1℃时,三种物质的溶解度大小顺序是:B>A=C,正确;
C、C的溶解度随温度升高而减小,所以其不饱和溶液变为饱和溶液可采取升温的方法,正确;
D、A的溶解度随温度升高而增大,B的溶解度受温度变化不大,所以A中混有少量B,可采用蒸发结晶的方法提纯B,故错误;
故选:D.
点评 掌握饱和溶液中溶质的质量分数的计算方法、溶解度曲线的意义等知识,并会应用知识解决相关问题.

练习册系列答案
相关题目
17.目前下列元素的质量分数,在人体中和地壳中含量最大的为( )
| A. | 氮 | B. | 氧 | C. | 碳 | D. | 氢 |
18.4.6g某化合物在足量氧气中充分燃烧,生成8.8g二氧化碳和5.4g水.下列对该化合物组成的判断中,正确的是( )
| A. | 由碳、氢两种元素组成 | |
| B. | 由碳、氧两种元素组成 | |
| C. | 由碳、氢、氧三种元素组成 | |
| D. | 一定含有碳、氢两种元素,可能含有氧元素 |
15.下列图象不能正确反映其对应关系的是( )
| A. | 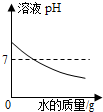 向氢氧化钠溶液中不断加水 | |
| B. | 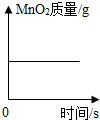 氯酸钾和二氧化锰混合加热制取氧气 | |
| C. |  向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 | |
| D. | 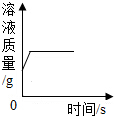 某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 |
12.关于 CaCO3的说法正确的是( )
| A. | 由钙、碳、氧三个元素组成 | B. | 碳元素的化合价为+2 | ||
| C. | 钙元素的质量分数为40% | D. | 属于氧化物 |
19.实验室要配置200g溶质质量分数为l0%的NaCl溶液,回答有关问题.
(l)计算:需要NaCl的质量为20g;
(2)称量:用托盘天平称量所需质量的NaCl固体:
(3)量取:用量筒量取水时,视线要与凹液面的最低点保持水平,如果俯视读数,会使配制成的溶液的浓度大于l0% (选填“大于”、“小于”或“等于”);
(4)溶解:在溶解时要使用玻璃棒搅拌,玻璃棒的作用是搅拌,加速溶解;
(5)装瓶并贴标签:将右侧的标签补充完整.
(l)计算:需要NaCl的质量为20g;
(2)称量:用托盘天平称量所需质量的NaCl固体:
(3)量取:用量筒量取水时,视线要与凹液面的最低点保持水平,如果俯视读数,会使配制成的溶液的浓度大于l0% (选填“大于”、“小于”或“等于”);
(4)溶解:在溶解时要使用玻璃棒搅拌,玻璃棒的作用是搅拌,加速溶解;
(5)装瓶并贴标签:将右侧的标签补充完整.
| NaCl溶液 |
| 溶质质量分数为l0% |
| 2016年3月10日 |
16.“一带一路”是跨越时空的宏伟构想,赋予古丝绸之路崭新的时代内涵,古丝绸之路将中国的发明和技术传送到国外,下列不属于化学变化的是( )
| A. | 稻草造纸 | B. | 使用火药 | C. | 冶炼金属 | D. | 蚕丝织绫 |
17. 甲、乙两种固体物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列说法正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,甲、乙饱和溶液中含溶质的质量相等 | |
| B. | t1℃时,甲、乙两种物质各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g | |
| C. | t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数 | |
| D. | t2℃时甲、乙的饱和溶液降温到t1℃时,折出晶体的质量甲一定大于乙 |