题目内容
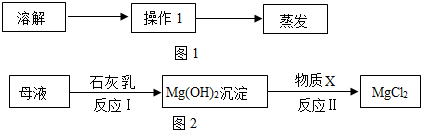
20.我省沿海城市拥有丰富的海洋资源,开发利用这些宝贵的资源有力地促进了我省经济的发展.(1)从海水中提取出的粗盐中除了NaCl外,还含有泥沙等杂质.实验室按如图1所示流程进行粗盐的初步提纯:
其中操作1的名称是过滤;在操作1中要用到的玻璃仪器有烧杯、玻璃棒和漏斗(填仪表名称).在加热蒸发过程中,当蒸发皿中出现较多量固体时,即停止加热.
(2)上述除去泥沙后的澄清滤液中,还含有Ca2+、Mg2+等阳离子,若要想知道该滤液是硬水还是软水,可加入肥皂水进行检验.
(3)从海水提取出粗盐后的母液中,还含有较多的氯化镁,用氯化镁可制得金属镁.工业上从母液中提取氯化镁的过程如图2所示:
反应1的化学方程式为MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;物质X的名称是稀盐酸.
(4)工业上用电解饱和NaCl溶液的方法制得烧碱、氯气和氢气,请写出该反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.已知:20℃时,S(NaCl)=36.0kg,现要将20℃时溶质的质量分数 为6.5%的NaCl不饱和溶液36.0kg转变为同温度下的饱和溶液,应至少加入NaCl固体9.8kg(计算结果精确到0.1kg)
分析 (1)根据粗盐提纯的步骤和仪器以及注意事项来分析解答;
(2)通常用肥皂水来检验硬水和软水;
(3)根据工艺流程来分析反应过程和所用原料;
(4)根据已知条件可知,电解饱和NaCl溶液,生成烧碱、氢气和氯气,据此写出化学方程式即可;根据溶解度来分析.
解答 解:解:(1)去除泥沙的步骤是:①溶解:把粗盐放入烧杯中,加水溶解;②过滤:架好漏斗,使漏斗下端口紧贴烧杯内壁,沿玻璃棒把上述悬浊液慢慢导入漏斗中;该过程中用到的玻璃仪器主要有烧杯、玻璃棒和漏斗等;③蒸发结晶:将上述滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多量晶体时即停止加热;
(2)硬水是指含有较多钙镁离子的水,软水是指含有较少钙镁离子的水.区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;
(3)反应Ⅰ氯化镁与氢氧化钙反应生成氯化钙和氢氧化镁沉淀,反应Ⅱ将碱转化成了盐,应该加入酸;
(4)工业生产通过电解饱和食盐水得到烧碱、氯气、氢气,反应的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
设需要加入氯化钠的质量为x,则
$\frac{36.0kg×6.5%+x}{x+36.0kg}=\frac{36.0g}{36.0g+100g}$
x=9.8kg
故答案为:(1)过滤;漏斗;较多量固体;(2)肥皂水;(3)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;稀盐酸;(4)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;9.8.
点评 海水的综合利用是初中化学中较为重要的内容之一,与之相关的实验操作,药品的选用,化学方程式的书写等都是经常考查的内容,同学们一定要对此内容了然于心.

| A. | 滤液中一定含有FeSO4 可能含有H2SO4 | |
| B. | 滤液中可能含有CuSO4 | |
| C. | 滤渣里一定有Fe 和Cu | |
| D. | 滤渣里一定有 Cu 可能有 Fe和CuO |
| A. | Fe3+、K+、NO3-、OH- | B. | H+、Na+、HCO3-、Cl- | ||
| C. | Ag+、NH4+、Cl-、SO42- | D. | Na+、K+、NO3-、CO32- |
| A. | 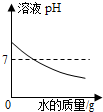 向氢氧化钠溶液中不断加水 | |
| B. | 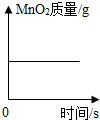 氯酸钾和二氧化锰混合加热制取氧气 | |
| C. |  向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液 | |
| D. | 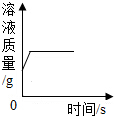 某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 |
| A. | 由钙、碳、氧三个元素组成 | B. | 碳元素的化合价为+2 | ||
| C. | 钙元素的质量分数为40% | D. | 属于氧化物 |
| A. | 羟喜树碱分子由碳元素、氢元素、氧元素、氮元素组成 | |
| B. | 羟喜树碱分子中碳的原子结构示意图为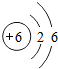 | |
| C. | 羟喜树碱中含有五氧化二氮 | |
| D. | 羟喜树碱中碳氢元素的质量比为15:1 |
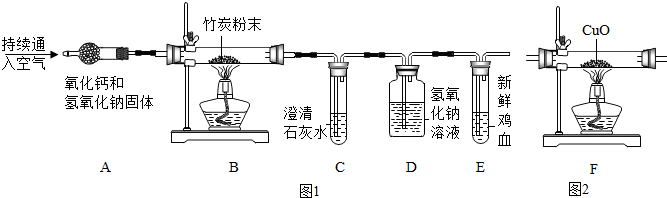
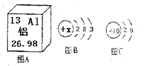 如图A是元素周期表中的一格,分析回答问题:
如图A是元素周期表中的一格,分析回答问题: