题目内容
11.某同学利用稀盐酸、氢氧化钡溶液、碳酸钠溶液、氯化钡溶液之间的下列反应,探究酸、碱、盐之间能发生哪些反应:A.HCl+Ba(OH)2 B.HCl+Na2CO3C.BaCl2+Na2CO3
(1)在实验A中,确定两种物质能够发生化学反应,最好借助的指示剂是:酚酞试液;
(2)实验B中发生反应的化学反应方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)在实验C中证明反应发生的实验现象:产生白色沉淀;
(4)将上述三个反应完成后所得到的物质混合在同一个烧杯中,发现有气泡冒出,一段时间后得到无色澄清的废液.综合分析有关反应和实验现象推断,所得废液中一定含有NaCl、BaCl2的溶质;
(5)关于(4)中废液的用途中不合理的是C.
A.利用废液制备氯化钠溶液:加入适量硫酸钠溶液制备氯化钠
B.检验氯化钠溶液中的碳酸钠:向其中加入过量废液检验其中是否有碳酸钠
C.检验某氢氧化钠固体是否完全变质:把固体溶解后,向其中加入过量该废液,观察现象.
分析 (1)根据氢氧化钡能使酚酞显红色,滴入稀盐酸后红色逐渐褪去,可以证明盐酸和氢氧化钡能够发生化学反应进行分析;
(2)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(3)根据氯化钡和碳酸钠反应会生成氯化钠和碳酸钡沉淀进行分析;
(4)根据氯化钡和碳酸钠会生成碳酸钡沉淀和氯化钠,碳酸钡沉淀和盐酸反应会生成氯化钡、水和二氧化碳进行分析;
(5)根据废液可能含有盐酸,盐酸会与碳酸钠和氢氧化钠反应而影响物质的检验进行分析.
解答 解:(1)氢氧化钡能使酚酞显红色,滴入稀盐酸后红色逐渐褪去,可以证明盐酸和氢氧化钡能够发生化学反应,所以最好借助的指示剂是酚酞试液;
(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)氯化钡和碳酸钠反应会生成氯化钠和碳酸钡沉淀,所以实验C中反应发生的实验现象为:产生白色沉淀;
(4)氯化钡和碳酸钠会生成碳酸钡沉淀和氯化钠,碳酸钡沉淀和盐酸反应会生成氯化钡、水和二氧化碳,所以反应完成后所得到的物质混合在同一个烧杯中,发现有气袍冒出,一段时间后得到无色澄清的废液,所得废液中一定含有的溶质:NaCl、BaCl2;
(5)A、硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,故A正确;
B、碳酸钠和氯化钡会生成碳酸钡沉淀和氯化钠,可以检验碳酸钠,故B正确;
C、废液可能含有盐酸,盐酸会与碳酸钠和氢氧化钠反应而影响氢氧化钠、碳酸钠的检验,故C错误.
故选:C.
故答案为:(1)酚酞试液;
(2)Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)产生白色沉淀;
(4)NaCl、BaCl2;
(5)C.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

| A. | 氨气在常压下液化是物理变化,液氨具有可燃性属于化学性质 | |
| B. | 在生成X的过程中化学能转化成热能,X为空气中含量最多的气体 | |
| C. | 该反应为置换反应 | |
| D. | 液氨属于混合物 |
面粉酸度与面粉品质的关系表
| 面粉酸度 | <2° | 2°-4.5° | >4.5° |
| 面粉品质 | 新鲜面粉 | 陈年面粉 | 霉变面粉 |
(1)为检测某种面粉中是否含有淀粉,取一定质量的面粉放入烧杯中,加入适量的蒸馏水,搅拌,缓缓加热,溶解,取少量试液置于试管中,滴加碘液,若溶液变蓝色,就说明该面粉中含有淀粉.
(2)称取5克某种面粉放入锥形瓶,加入适量蒸馏水搅匀,为减小实验误差,现用质量分数为0.004%氢氧化钠溶液来进行测定,恰好完全反应时共消耗22毫升氢氧化钠溶液.计算该面粉的酸度4.4°;,并判断其品质(忽略两种氢氧化钠溶液密度的差异)陈年面粉.
(09佛山)已知某合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究。
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应。
【猜 想】猜想1:该合金粉末中除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有 (填名称)。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
实验方案 | 实现现象 | 结论 |
①取一定量的合金粉末,加过量的 ,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气体放出。 | 合金中一定含有 。 |
②取步骤①所得滤渣,加过量的 ,充分反应。 | 滤渣部分溶解,并有气体放出,溶液呈浅绿色。 | 合金中一定含有 。 |
【探究结论】猜想3成立。
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。写出铝与稀盐酸反应的化学方程式 。
①2CuO+C $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ ②CuO+C $\frac{\underline{\;高温\;}}{\;}$Cu+CO↑
他们想来自己的想法,请你同他们一起进行探究:
[猜想与假设]
木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;(2)产物是铜和二氧化碳;(3)产物是铜和一氧化碳、二氧化碳
[设计方案]
(1)检验产物中是否有CO2的方法是(用化学方程式表示)Ca(OH)2+CO2═CaCO3↓+H2O;
(2)如何检验产物中是否存在CO,两人查找了资料:CO的特征反应是CO能使某种氯化钯的黄色混合液变蓝.CO有毒、有可燃性.
[实验与结论]
设计的实验装置(见图1)
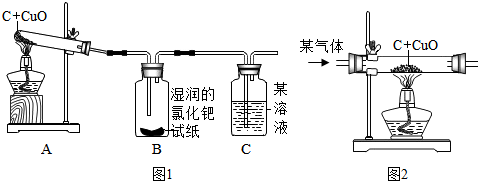
实验报告:
| 实验现象 | 实验结论 |
| ①A中固体由黑色变红色 ②B中黄色试纸变蓝 ③C中澄清石灰水变浑浊 | ①有Cu生成 ②有CO生成 ③有CO2生成 |
①实验结束时,为防止铜被氧化,必须先停止加热,待铜冷却后再将试管口的胶塞取下,因此若没有B安全瓶,可能导致的后果是液体倒吸入试管把试管炸裂.
②根据实验结论,从环保角度考滤,上述装置C后应添加的装置是酒精灯,或塑料袋.
[拓展与交流]如果用图2装置代替图1中的A装置,这样既可以排尽试管中的空气,又能将反应的气体产物都“赶”出来,该气体可以是B (A.空气 B.氮气 C.氧气 )
 图一是元素周期表中磷元素的部分信息,图二是该元素的某种微粒的结构示意图.
图一是元素周期表中磷元素的部分信息,图二是该元素的某种微粒的结构示意图.