题目内容
3.某学校化学兴趣小组同学小博经查阅资料知道,FeSO4•7H2O是一种重要的食品和饲料添加剂.为此小组同学开始探索工业制备FeSO4•7H2O的过程,选择了某工来废渣主要成分是Fe2O3,还含有CaCO3和SiO2(既不溶于水也溶于稀硫酸).请根据流程图回答下列问题:
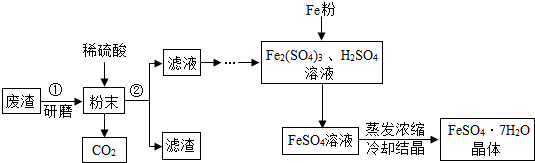
(1)操作①中将废渣变成粉末的目的是增大与稀硫酸的接触面积,使反应更充分,稀硫酸与粉末中的氧化铁反应的化学方程式为Fe2O3+2H2SO4═Fe2(SO4)3+3H2O.
(2)操作②所需要的玻璃仪器是:烧杯、玻璃棒和漏斗.固定装置是铁架台.
(3)经测定,滤渣中只含CaCO3和SiO2,你认为实验室能(填“能”或者“不能”)用粉末的石灰石与稀硫酸反应制二氧化碳.
(4)Fe与Fe2(SO4)3反应生成FeSO4的化学方程式为Fe+Fe2(SO4)3═3FeSO4,反应中化合价发生变化的元素是Fe.
(5)硫酸亚铁的溶解度曲线如图2,待结晶完毕后,滤除晶体,用少量冰水洗涤2~3次.用冰水洗涤的目的是(结合硫酸亚铁的溶解度曲线图进行分析):
Ⅰ.除去晶体表面附着的杂质;Ⅱ.用冰水洗涤可降低洗涤过程中FeSO4•7H2O的损耗.

分析 (1)根据增大接触面积可以加快反应速率,稀硫酸与粉末中的氧化铁反应生成硫酸铁和水去进行分析;
(2)根据过滤可以将固体和液体分离,过滤需用到的仪器有:烧杯、玻璃棒和漏斗去进行分析;
(3)根据测定,滤渣中只含有CaSO4和SiO2;说明废渣中的碳酸钙已经完全和稀硫酸反应,生成了二氧化碳气体去分析解答;
(4)从图可知:Fe与Fe2(SO4)3反应生成FeSO4,反应物是Fe和Fe2(SO4)3,生成物是FeSO4去分析解答;
(5)从硫酸亚铁的溶解度曲线如图1可以看出:硫酸亚铁的溶解度随温度的升高而增大,冰水的温度低,硫酸亚铁在低温下的溶解度小,可降低洗涤过程中绿矾的溶解而造成的损失去分析解答.
解答 解:(1)将废渣研磨的目的是:增大与稀硫酸的接触面积,使反应更充分,稀硫酸与粉末中的氧化铁反应,生成硫酸铁和水,化学方程式为:Fe2O3+2H2SO4═Fe2(SO4)3+3H2O;
(2)由题目中图可以看出步骤②用来分离固体和液体,获得滤液和滤渣,所以这个步骤是过滤;过滤时需用到的仪器有:烧杯、玻璃棒和漏斗;固定装置是铁架台;
(3)工业废渣主要成分是Fe2O3,还含有CaCO3和SiO2(既不溶于水也不溶于稀硫酸),加入稀硫酸后,题目中指出:“经测定,滤渣中只含有CaSO4和SiO2;”说明废渣中的碳酸钙已经完全和稀硫酸反应,生成了二氧化碳气体;
(4)由图可知:Fe与Fe2(SO4)3反应生成FeSO4,反应物是Fe和Fe2(SO4)3,生成物是FeSO4,故反应的化学方程式为:Fe+Fe2(SO4)3═3FeSO4;反应前后,铁元素由0价、+3价转化为+2价,硫元素和氧元素的化合价没有改变;
(5)硫酸亚铁的溶解度曲线如图1可以看出:硫酸亚铁的溶解度随温度的升高而增大,用冰水洗涤的目的是一、除去晶体表面附着的溶于水杂质,二、冰水的温度低,硫酸亚铁在低温下的溶解度小,可降低洗涤过程中绿矾的溶解而造成的损失.
故答案为:(1)增大与稀硫酸的接触面积,使反应更充分;Fe2O3+2H2SO4═Fe2(SO4)3+3H2O;
(2)漏斗;铁架台;
(3)能;
(4)Fe+Fe2(SO4)3═3FeSO4;Fe;
(5)用冰水洗涤可降低洗涤过程中FeSO4•7H2O的损耗.
点评 块状的石灰石和稀硫酸反应时,由于生成的硫酸钙微溶于水,附着在碳酸钙的表面,阻止了碳酸钙与稀硫酸的进一步接触,使反应停止;而用碳酸钙粉末则增大了与稀硫酸的接触面积,避免上述现象,反应得以进行,故可用碳酸钙粉末和稀硫酸制取二氧化碳气体.

| A.物质组成的差异性决定物质性质的差异性 | B.实验安全注意事项 |
| 金刚石与石墨---元素种类不同 一氧化碳与二氧化碳---分子构成不同 | 制取气体-先检查装置的气密性 点燃可燃性气体-先检验气体的纯度 |
| C.化学物质中的“三” | D.化学物质与俗名 |
| 三大化石燃料-煤、石油、天然气 三种黑色物质-氧化铜、二氧化锰、三氧化二铁 | 氧化钙-生石灰 碳酸钠-纯碱 |
| A. | 燃烧过程伴随着发光发热,所以有发光发热现象的变化一定是燃烧 | |
| B. | 有机物都含碳元素,所以含碳元素的化合物一定是有机物 | |
| C. | 氧化物都含氧元素,所以含氧元素的化合物都是氧化物 | |
| D. | 碱性溶液能使酚酞变红,所以使酚酞变红的溶液一定呈碱性 |
| A. | 离子是带电的原子和原子团,所以带电的粒子就是离子 | |
| B. | 化学变化都遵守质量守恒定律,所以质量不发生改变的变化就是化学变化 | |
| C. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 23 | 60 | 44 | 0 |
| 反应后的质量/g | 待测 | 12 | 88 | 27 |
| A. | 反应后X的质量为0g | |
| B. | 该反应生成的二氧化碳和水的质量比为88:27 | |
| C. | 物质X的化学式一定为C2H6O | |
| D. | 该反应属于置换反应 |
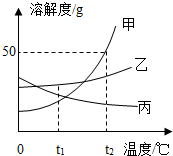 如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:
如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题: