题目内容
1.表是部分元素的原子结构示意图、主要化合价等信息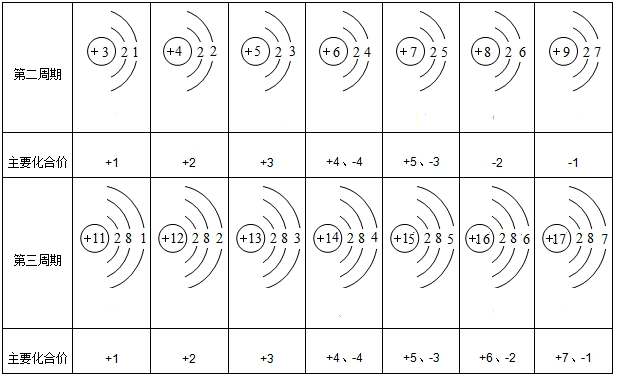
请完成以下填空:
(1)铝原子的最外层电子数是3.
(2)核电荷数为12元素符号是Mg.
(3)原子序数为8和14的元素组成化合物的化学式SiO2
(4)请你总结出此表中的原子结构与元素化合价或周期数的关系周期数=电子层数 (任写一条)
分析 (1)从铝元素的原子结构示意图可直观看出答案;
(2)根据元素符号可写出元素名称;
(3)根据两种元素的化合价可以写出其组成化合物的化学式;
(4)从题目表中给出的每周期元素的原子结构示意图和化合价可判断出之间的关系.
解答 解:(1)从铝元素的原子结构示意图可直接看出:铝原子的最外层电子数为3,故答案为3;
(2)从题目的表中看到核电荷数是12元素符号为Mg,所以名称是镁,故答案为Mg;
(3)根据题目的表中看到,原子序数为8的元素是氧元素,化合价为-2价;原子序数为14的元素是硅元素,化合价为+4、-4价.硅和氧结合硅显+4价,化合物为二氧化硅,故答案为SiO2
(4)从表中给出的每周期元素的原子结构示意图和化合价可看出,原子结构和元素化合价的关系是:最外层电子数=正化合价数,负化合价数=8-最外层电子数;原子结构和周期数的关系是:周期数=电子层数.
答案:
(1)3;(2)Mg;(3)SiO2;(4)周期数=电子层数.
点评 本题主要考查原子结构示意图、根据化合价书写化学式以及原子结构与化合价、周期数的关系,前两问较简单,后两问稍微有点难度.

练习册系列答案
相关题目
16.下列事实及对这些事实的解释,二者不相符合的是( )
| A. | 金属导电 原子是运动的 | |
| B. | 夏天钢轨之间的缝隙变小 原子之间有间隔 | |
| C. | 糖是甜的,醋是酸的 不同分子性质不同 | |
| D. | 电解水制取氢气和氧气 分子在化学反应中可以再分 |
13.在一个密闭容器中放入a、b、c、d四种物质,在一定条件下发生化学反应,反应前后,测得的有关数据如下表所示,则下列说法中正确的是B
A.表中未测值为0
B.a、c、d三种物质中所含元素与b的组成元素完全相同
C.反应中c、d的化学计量数之比为1:2
D.如果反应中a、d的微粒个数之比为1:1.则a、d的相对原子质量之比为17:44.
| 物质 | a | b | c | d |
| 反应前质量/g | 未测 | 7.9 | 1 | 2 |
| 反应后质量/g | 3.7 | 0 | 2.8 | 6.4 |
B.a、c、d三种物质中所含元素与b的组成元素完全相同
C.反应中c、d的化学计量数之比为1:2
D.如果反应中a、d的微粒个数之比为1:1.则a、d的相对原子质量之比为17:44.
20.合金的用途十分广泛.某化学兴趣小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如表所示.请计算:
(1)黄铜片中铜的含量.
(2)稀硫酸中参加反应的硫酸的质量是多少?(小数点后保留一位有效数字)
| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 23.5 | 17 | 10.5 | 9.6 | 9.6 |
(2)稀硫酸中参加反应的硫酸的质量是多少?(小数点后保留一位有效数字)
6.下列实验操作中,正确的是( )
| A. | 给试管里的液体加热.液体体积不超过试管容积的$\frac{2}{3}$ | |
| B. | 将实验剩余的药品及时放回原试剂瓶 | |
| C. | 用酒精灯给试管内物质加热,试管的底部与灯芯接触 | |
| D. | 将颗粒状石灰石装入试管时,让石灰石缓缓地沿试管内壁滑到底部 |
10.在氯酸钾里加入少量的高锰酸钾,加热制氧的速率大大加快,其主要原因是( )
| A. | 高锰酸钾起了催化作用 | |
| B. | 高锰酸钾受热分解,使产生的氧气量大大增加 | |
| C. | 高锰酸钾受热分解生成的二氧化锰成为氯酸钾分解的催化剂 | |
| D. | 高锰酸钾比氯酸钾容易分解 |
11.下列化学方程式书写正确的是( )
| A. | 2Fe+3H2SO4═Fe2(SO4)3+3H2↑ | B. | Cu+AgNO3═Cu(NO3)2+Ag | ||
| C. | CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | D. | CaCO3+2HCl═CaCl2+H2O+CO2 |

 ”和“
”和“ ”与反应后生成的“
”与反应后生成的“ ”各粒子间的个数比为2:1:2;
”各粒子间的个数比为2:1:2;