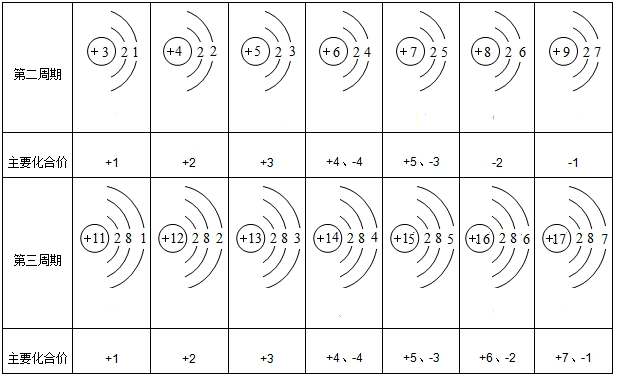
题目内容
20.合金的用途十分广泛.某化学兴趣小组欲测定黄铜片(铜锌合金)的组成进行如下实验:取黄铜片30g放入烧杯,将250g稀硫酸分5次加入烧杯中,充分反应后,测得剩余固体的质量记录如表所示.请计算:| 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 23.5 | 17 | 10.5 | 9.6 | 9.6 |
(2)稀硫酸中参加反应的硫酸的质量是多少?(小数点后保留一位有效数字)
分析 根据锌会与硫酸反应生成硫酸锌和氢气,铜不会与稀硫酸反应,依据题中的数据进行计算.
解答 解:由表中数据知,合金中铜的质量为9.6g,其含量为:$\frac{9.6g}{30g}$×100%=32%,
与50g稀硫酸完全反应消耗锌的质量为:30g-23.5g=6.5g,
设与6.5g锌反应的硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑,
65 98
6.5g x
$\frac{65}{6.5g}=\frac{98}{x}$
x=9.8g
故:(1)黄铜片中铜的含量是32%,(2)稀硫酸中参加反应的硫酸的质量是9.8g.
点评 本题主要考查化学方程式进行计算,计算时要注意规范性和准确性.

练习册系列答案
相关题目
10.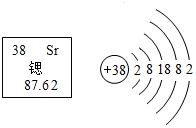 据媒体报道,锶晶体各钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒,如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体各钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒,如图为锶元素的相关信息,下列说法正确的是( )
 据媒体报道,锶晶体各钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒,如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体各钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒,如图为锶元素的相关信息,下列说法正确的是( )| A. | 原子核内中子数为87 | B. | 该元素的相对原子质量为87.62克 | ||
| C. | 锶易失去电子,其离子符号为Sr2+ | D. | 锶属于非金属元素,位于第五周期 |
11.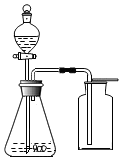 使用如图装置可以进行下列实验中的( )
使用如图装置可以进行下列实验中的( )
 使用如图装置可以进行下列实验中的( )
使用如图装置可以进行下列实验中的( )| A. | 锌与稀硫酸制取、收集氢气 | |
| B. | 石灰石与稀硫酸制取、收集二氧化碳 | |
| C. | KMnO4制取、收集氧气 | |
| D. | 过氧化氢溶液与MnO2制取、收集氧气 |
8.下列生活现象中,属于化学变化的是( )
| A. | 糖溶解到水中 | B. | 铁锈蚀 | ||
| C. | 通电后灯泡发光了 | D. | 湿衣服晾干了 |
5.九月的怀文校园,鲜花盛开,香远益清,阵阵花香,沁人心脾.花香四溢的现象说明( )
| A. | 分子具有质量 | B. | 分子可以分解成原子 | ||
| C. | 分子体积很小 | D. | 分子在不断地运动 |
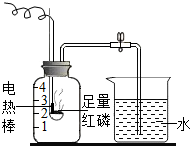 某化学兴趣小组的同学用如图所示的装置测定空气中氧气的含量,请回答下列问题:
某化学兴趣小组的同学用如图所示的装置测定空气中氧气的含量,请回答下列问题: