题目内容
14. 实验欲配制50g质量分数为5%的食盐溶液.试回答下列问题:
实验欲配制50g质量分数为5%的食盐溶液.试回答下列问题:(1)该实验的操作步骤为计算、称量、量取、溶解.
(2)请分别说明图中A、B操作对实验结果的影响,并加以改正.
A操作导致所配制的溶液的质量分数偏小(填“偏大”、“偏小”或“不变”),改正应将药品放在左盘,砝码放在右盘;
B操作导致所配制的溶液的质量分数偏大(填“偏大”、“偏小”或“不变”),改正量筒读数时视线要与量筒内液体的凹液面的最低处保持水平.
(3)托盘天平称量完毕后,砝码应放回砝码盒,游码应归零.
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(2)从溶质质量分数的概念入手,与溶质和溶剂的质量有关,分析操作中的错误操作,判断错误操作对溶质、溶剂的影响.
(3)根据托盘天平的使用注意事项解答.
解答 解:(1)配制50g5%的NaCl溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解.
(2)用托盘天平称量食盐时,砝码和食盐放反了,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小;应将药品放在左盘,砝码放在右盘.
用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大;
(3)托盘天平称量完毕后,砝码应放回砝码盒,游码应归零.
故答案为:
(1)计算、称量、量取、溶解;
(2)偏小;应将药品放在左盘,砝码放在右盘;偏大;量筒读数时视线要与量筒内液体的凹液面的最低处保持水平.
(3)放回砝码盒;归零.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
5.在一定条件下,同一反应进行的快慢与反应物的质量分数成正比.现用100g溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点进行又不影响生成氢气的总质量,可向所用的硫酸溶液中加入适量的( )
| A. | 氢氧氢钠 | B. | 水 | C. | 氧化镁 | D. | 氯化钠溶液 |
19.下列实验操作或现象的描述正确的是( )
| A. | 将50.0mL酒精与50.0mL蒸馏水混合,所得溶液体积小于100.0mL | |
| B. | 铁丝在氧气中燃烧,剧烈燃烧、火星四射、放热,生成四氧化三铁 | |
| C. | “粗盐提纯”实验中,过滤时将悬浊液直接倒入漏斗 | |
| D. | 硫在空气中燃烧发出明亮蓝紫色火焰,生成无色无味气体 |
6.如图所示图象不正确的是 ( )
| A. | 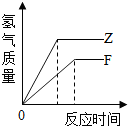 表示向足量的稀HCl中加入等质量的锌和铁,生成氢气质量和反应时间的关系图 | |
| B. | 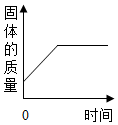 表示CO还原Fe2O3的实验中,试管内的固体质量与时间的关系图 | |
| C. | 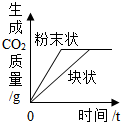 表示等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 | |
| D. |  表示向足量的稀HCl中加入少量Fe,溶液质量与时间的关系图 |
2.下列装置或操作能达到实验目的是( )
| A. |  收集CO2 | B. |  验证CO2性质 | ||
| C. |  比较MnO2和Fe2O3的催化效果 | D. |  测定反应产生O2的速率 |

 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子.
”表示氧原子. ”可表示的微粒是氮分子(填微粒名称).
”可表示的微粒是氮分子(填微粒名称).