题目内容
5.在一定条件下,同一反应进行的快慢与反应物的质量分数成正比.现用100g溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点进行又不影响生成氢气的总质量,可向所用的硫酸溶液中加入适量的( )| A. | 氢氧氢钠 | B. | 水 | C. | 氧化镁 | D. | 氯化钠溶液 |
分析 (1)在此题中,硫酸溶液与镁粉反应生成氢气全部来自于硫酸,硫酸质量分数的大小决定了化学反应的快慢,硫酸的质量多少决定了生成氢气质量多少.
(2)同一化学反应进行的快慢与反应物的质量分数成正比,就要考虑影响硫酸溶液分数的因素;生成氢气的质量多少就要考虑硫酸溶液的质量是否发生了改变.
解答 解:A、氢氧化钠与硫酸溶液反应,硫酸溶液质量减少了,因为氢气中的氢全部来自酸,所以生成氢气的质量减少,故不选;
B、加水等于稀释硫酸,降低了硫酸溶液的质量分数,与镁反应减缓进行,而硫酸溶液质量没有改变,所以生成氢气的质量没有改变,故选;
C、加入氧化镁,氧化镁能和硫酸溶液反应,降低了硫酸溶液质量分数和质量,与镁减缓反应,生成氢气的质量减少,故不选;
D、氯化钠与硫酸溶液反应,硫酸溶液质量减少了,因为氢气中的氢全部来自酸,所以生成氢气的质量减少,故不选;
故选B.
点评 从此题可以看出,改变硫酸溶液质量分数的不只是溶液中溶质、溶剂和溶液的质量,还分析一下,加入物质是不是与硫酸溶液发生反应.如果反应,硫酸溶液的质量会减小,硫酸溶液的质量分数也会减小,不仅影响反应的快慢,也会影响生成氢气的多少,所以要求学生能够将所学知识进行综合,在平时的学习和训练中培养学生综合分析问题能力是非常重要的.

练习册系列答案
相关题目
13.对比是学习化学的重要方法,下列关于H2O2与H2O的比较,错误的是( )
| A. | 两种物质都适用于在实验室中制取氧气 | |
| B. | 两种物质都属于氧化物 | |
| C. | H2O2与H2O组成元素相同,但氧元素化合价不同 | |
| D. | 一个过氧化氢分子比一个水分子多一个氧原子 |
20.下列做法或举措中与爱护水资源无关的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
13.属于分解反应的是( )
| A. | CuSO4+2NaOH→Na2SO4+Cu(OH)2↓ | B. | H2CO3$\stackrel{△}{→}$H2O+CO2↑ | ||
| C. | CaCO3+H2O+CO2→Ca(HCO3)2 | D. | 2Mg+CO2$\stackrel{点燃}{→}$2MgO+C |
 如图是几种常见物质之间的转化关系,其中“→”表示转化,转化条件及其他物质都已省略.
如图是几种常见物质之间的转化关系,其中“→”表示转化,转化条件及其他物质都已省略.
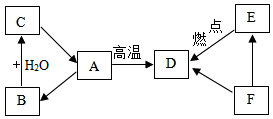 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F 三种物质含有同种非金属元素,其中E与血红蛋白的结合力大约是氧气的200~300倍,F是单质.将A高温煅烧,得到B与D,它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F 三种物质含有同种非金属元素,其中E与血红蛋白的结合力大约是氧气的200~300倍,F是单质.将A高温煅烧,得到B与D,它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答: 医生给病人输液时,常用葡萄糖注射液,如图为葡萄糖注射液的部分标签图,请计算:
医生给病人输液时,常用葡萄糖注射液,如图为葡萄糖注射液的部分标签图,请计算: 实验欲配制50g质量分数为5%的食盐溶液.试回答下列问题:
实验欲配制50g质量分数为5%的食盐溶液.试回答下列问题: