题目内容
17.红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,品名:504 双吸剂成分:铁粉、石灰其标签如右图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究.【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁,氯化亚铁溶液的颜色为浅绿色.
【作出猜想】久置固体中可能含有 Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【实验探究】
(1)为验证固体中 CaCO3是否存在,你采用的实验方法是取固体加盐酸,将产生的气体通入石灰水中.如果该物质存在,对应的现象和结论是有气体产生,石灰水变浑浊.
(2)某同学取少量固体混合物投入水中,滴加酚酞后溶液变红,由此他认为固体中有Ca(OH)2,他的判断正确吗?请说明理由不正确,因为也可能是氧化钙与水反应生成了碱--氢氧化钙.
(3)某同学取少量固体混合物投入盐酸中,发现固体溶解后溶液呈浅绿色而不是黄色,他由此断定固体中不存在 Fe2O3,但肯定存在铁.你认为他的结论正确吗?为什么?不正确,氧化铁有可能存在.与盐酸反应生成的氯化铁又与铁反应变成了氯化亚铁,所以看不到黄色溶液.
(4)要判断固体中是否有 CaO 存在,可采用的方法是把固体放入水中,若产生大量热说明有CaO.
分析 (1)根据碳酸盐的检验方法来分析;
(2)氧化钙能与水反应生成氢氧化钙;
(3)根据氯化铁能与铁反应生成氯化亚铁来进行分析;
(4)根据氧化钙与水反应放出热量进行分析.
解答 解:(1)为验证固体中 CaCO3是否存在,可取固体加稀盐酸,将产生的气体通入石灰水中,若观察到有气体产生,石灰水变浑浊,说明其中含有碳酸钙;故填:取固体加稀盐酸,将产生的气体通入石灰水中;有气体产生,石灰水变浑浊;
(2)因为氧化钙能与水反应生成氢氧化钙,此时滴加酚酞试液也会观察到溶液变红,所以此判断不正确;故填:不正确,因为也可能是氧化钙与水反应生成了碱--氢氧化钙.
(3)氧化铁与稀盐酸反应生成氯化铁和水,氯化铁与铁反应生成浅绿色的氯化亚铁溶液,所以看不到黄色;故填:不正确,氧化铁有可能存在.与盐酸反应生成的氯化铁又与铁反应变成了氯化亚铁,所以看不到黄色溶液.
(4)因为氧化钙与水反应生成氢氧化钙,并且会释放出大量的热,故可用此方法来进行检验,故填:把固体放入水中,若产生大量热说明有CaO.
点评 有关实验方案的设计是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法,本考点主要出现在实验题中.

练习册系列答案
相关题目
5.下图是实验室制取某些常见气体的装置图.根据所学知识回答:
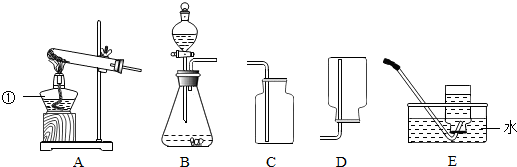
(1)写出仪器①的名称酒精灯;
(2)实验室用块状碳酸钙和稀盐酸制取二氧化碳,可选用B作为发生装置,选用C作为收
集装置.
(3)为了确定碳酸钙和稀盐酸反应后溶液的成分,小黄同学取用一定量的该溶液,向其中逐渐加入
一定质量分数的碳酸钠溶液,得到沉淀的质量与所加碳酸钠溶液的质量关系如下表所示:
分析数据可知:碳酸钙和稀盐酸反应后的溶液中的溶质是CaCl2(氯化钙)和HCl;表格中X为4克;
计算所加碳酸钠溶液的溶质质量分数?(写出计算过程)

(1)写出仪器①的名称酒精灯;
(2)实验室用块状碳酸钙和稀盐酸制取二氧化碳,可选用B作为发生装置,选用C作为收
集装置.
(3)为了确定碳酸钙和稀盐酸反应后溶液的成分,小黄同学取用一定量的该溶液,向其中逐渐加入
一定质量分数的碳酸钠溶液,得到沉淀的质量与所加碳酸钠溶液的质量关系如下表所示:
| 加入Na2CO3溶液的质量/克 | 20 | 40 | 60 | 80 | 100 |
| 生成沉淀的质量/克 | 0 | 1 | 3 | 4 | X |
计算所加碳酸钠溶液的溶质质量分数?(写出计算过程)
2.下列各组物质充分混合后?能得到溶液的是( )
| A. | 泥沙加入水中 | B. | 酒精加入水中 | C. | 花生油加入水中 | D. | 冰加入水中 |
9.某有机物在氧气中完全燃烧?只生成二氧化碳和水.由此推知该有机物( )
| A. | 一定含碳、氢、氧元素 | B. | 一定含碳、氢元素,可能含氧元素 | ||
| C. | 只含碳、氢元素 | D. | 无法确定 |
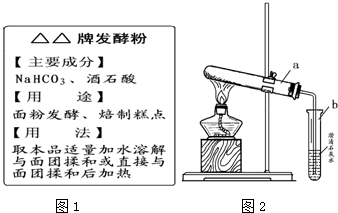
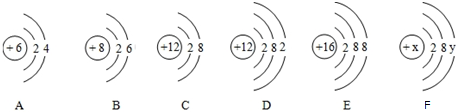
 根据如图中标签上信息填空:
根据如图中标签上信息填空: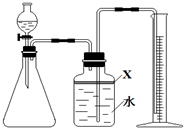 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.