题目内容
8.根据下列粒子结构示意图完成下列问题: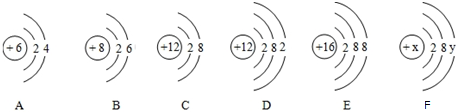
(1)上述粒子中属于阳离子的是C,属于同种元素的粒子是C、D.
(2)上述粒子中原子有A、B、D.
(3)写出E所表示的化学元素的符号S2-.
(4)若图F所示的原子中y=4,则x=14.
分析 (1)根据由于在阳离子中:质子数>电子数,元素是指具有相同的核电荷数(即质子数)的一类原子的总称进行解答;
(2)根据原子中质子数等于核外电子数进行解答;
(3)根据E中质子数为16,核外电子数为18,所以为硫离子进行解答;
(4)根据原子中质子数等于核外电子数进行解答.
解答 解:(1)由于在阳离子中:质子数>电子数,所以上述粒子中属于阳离子的是C;元素是指具有相同的核电荷数(即质子数)的一类原子的总称,所以属于同种元素的粒子是C、D,质子数都是12;
(2)原子中质子数等于核外电子数,所以上述粒子中原子有A、B、D;
(3)E中质子数为16,核外电子数为18,所以为硫离子,离子符号为S2-;
(4)原子中质子数等于核外电子数,所以x=2+8+4=14.
故答案为:(1)C;C、D;(2)A、B、D;(3)S2-;(4)14.
点评 主要考查了原子、离子结构示意图的意义,及离子所带电荷间的关系,培养学生分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.一次性鉴别开氧气、氮气和空气三瓶气体,最好选用( )
| A. | 带火星的木条 | B. | 燃着的木条 | C. | 澄清石灰水 | D. | 燃着的木炭 |
19.有人用石灰乳刷墙,开始时,墙面变得潮湿,过几天墙面变得又硬又白了.其反应原理为:Ca(OH)2+CO2=CaCO3↓+H2O.则下列说法中,正确的是( )
| A. | 刷墙所用的石灰乳属于溶液,其溶质是氢氧化钙 | |
| B. | 氢氧化钙俗称熟石灰,受热分解可得到生石灰 | |
| C. | 一段时间后,墙面表层物质的PH比其内层物质的PH大 | |
| D. | 为了验证碳酸盐的生成,可用稀盐酸,澄清石灰水进行检验 |
3.实验室用高锰酸钾制取氧气,下列相关装置及操作正确的是( )
| A. |  发生装置 | B. |  排水法收集氧气 | C. |  验满 | D. |  存放氧气 |
20.宇宙飞船可用铝粉与高氯酸铵(NH4ClO4)的固体混合物作燃料,点燃时,铝粉被氧化放热引发高氯酸铵分解,其化学方程式为:2NH4ClO4 $\frac{\underline{\;\;△\;\;}}{\;}$N2↑+4H2O+Cl2↑+2O2↑.下列对此反应的叙述错误的是( )
| A. | 该反应属于分解反应 | |
| B. | 该反应产生大量高温气体,推动飞船飞行 | |
| C. | 该反应中有能量形式上的转化 | |
| D. | 在反应中铝粉是该反应的催化剂 |
18.空气是一种宝贵的自然资源.下列有关空气及成分说法中错误的是( )
| A. | 空气的主要成分是氮气和氧气 | |
| B. | 氮气的化学性质不活泼,可用于食品防腐 | |
| C. | 空气中可吸入颗粒物的多少不会影响人体健康 | |
| D. | 稀有气体通电时能发出不同颜色的光,可用作电光源 |
 红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如右图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如右图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究.