题目内容
11.在20℃时,取下表中的四种物质各20克,加入到100克水中充分溶解后,有固体剩余的是氯酸钾(填物质名称),要使这些剩余的固体物质继续溶解,可以采用的方法有升高温度或增加溶剂.| 常见物质的溶解度(20℃) | ||||
| 物质名称 | 氯酸钾 | 硝酸钾 | 氯化钠 | 蔗糖 |
| 溶解度/克 | 7.4 | 31.6 | 36.0 | 203.9 |
分析 根据20℃时,四种物质的溶解度,由溶解度的含义判断20℃时,20克四种物质加入到100克水中充分溶解的质量,结合饱和溶液与不饱和溶液的转化方法,进行分析解答.
解答 解:在20℃时,取下表中的四种物质各20克,加入到100克水中充分溶解后,氯酸钾的溶解度为7.4g,即该温度下100g水中最多溶解7.4g氯酸钾,则有固体剩余的是氯酸钾.
要使这些剩余的固体物质继续溶解,可采用升高温度或增加溶剂的方法.
故答案为:氯酸钾;升高温度或增加溶剂.
点评 本题难度不大,掌握饱和溶液的特征、溶解度的概念、饱和溶液与不饱和溶液的相互转化是正确解答本题的关键.

练习册系列答案
相关题目
5.下表是部分物质的溶解性表(室温),利用表中提供的信息完成下列问题:
(1)NaCl和K2CO3两种物质混合后不能(填“能”或“不能”)发生反应,理由是交换成分没有沉淀、气体或水生成,不符合复分解反应发生的条件.
(2)利用表中阴离子和阳离子构成的物质,写出一个有AgCl生成的化学方程式AgNO3+NaCl=NaNO3+AgCl↓(或AgNO3+KCl=KNO3+AgCl↓).
| NO3- | Cl- | CO32- | |
| Na+ | 溶 | 溶 | 溶 |
| K+ | 溶 | 溶 | 溶 |
| Ag+ | 溶 | 不 | 不 |
(2)利用表中阴离子和阳离子构成的物质,写出一个有AgCl生成的化学方程式AgNO3+NaCl=NaNO3+AgCl↓(或AgNO3+KCl=KNO3+AgCl↓).
2.下表中甲组物质能够与乙组物质全部反应的一组是( )
| 选项 | 甲 | 乙 |
| A | 稀硫酸 | 铜、氧化铜、氢氧化铜 |
| B | 氢氧化钙 | 二氧化碳、稀盐酸、碳酸钠 |
| C | 硫酸铜 | 铁、氢氧化钠、稀盐酸 |
| D | 铁 | 硝酸银、硫酸铜、氧化铝 |
| A. | A | B. | B | C. | C | D. | D |
3.下列过程中发生了化学变化的是( )
| A. | 海水晒盐 | B. | 麻线织布 | C. | 牛奶变酸 | D. | 浓盐酸挥发 |
20.在配制一定溶质质量分数的氯化钠溶液的实验中,下列实验操作不正确的是( )
| A. |  氯化钠的取用 | B. |  氯化钠的称量 | C. |  水的取用 | D. |  氯化钠的溶解 |
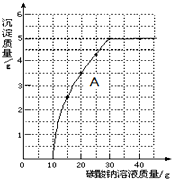 实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题: