题目内容
2.下表中甲组物质能够与乙组物质全部反应的一组是( )| 选项 | 甲 | 乙 |
| A | 稀硫酸 | 铜、氧化铜、氢氧化铜 |
| B | 氢氧化钙 | 二氧化碳、稀盐酸、碳酸钠 |
| C | 硫酸铜 | 铁、氢氧化钠、稀盐酸 |
| D | 铁 | 硝酸银、硫酸铜、氧化铝 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据题意,选择的是甲组物质能够与乙组物质全部反应的一组;据此结合酸、碱、盐与金属的化学性质,进行分析判断即可,可选用排除法(只要分析乙组中的一种物质与甲组的物质不反应,即可该选项)进行解答.
解答 解:A、铜的金属活动性比氢弱,不能与稀硫酸反应,故选项错误.
B、氢氧化钙与二氧化碳反应生成碳酸钙和水,与稀盐酸发生中和反应生成氯化钙和水,与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,甲组物质能够与乙组物质全部反应,故选项正确.
C、铁能与硫酸铜反应生成硫酸亚铁溶液和铜,硫酸铜与氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,硫酸铜与稀盐酸交换成分没有沉淀、气体或水生成,不能发生复分解反应,故选项错误.
D、铁能与硝酸银、硫酸铜溶液发生置换反应,铁不能与氧化铝反应,故选项错误.
故选:B.
点评 本题难度不大,掌握酸碱盐与金属的化学性质并能灵活运用是正确解答本题的关键;选用排除法是正确快速解答本题的捷径.

练习册系列答案
相关题目
12.某兴趣小组用氯酸钾和二氧化锰混合加热制取氧气,实验过程中,同学们统计了试管中固体的质量随时间变化的情况,具体数据见下表.试验结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.
试计算:
(1)实验中共制得氧气19.2g.
(2)所得氯化钾溶液的溶质质量分数是多少?
(3)回收的二氧化锰固体的质量为7.0g.
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 56.0 | 46.4 | 36.8 | 36.8 |
(1)实验中共制得氧气19.2g.
(2)所得氯化钾溶液的溶质质量分数是多少?
(3)回收的二氧化锰固体的质量为7.0g.
11.在20℃时,取下表中的四种物质各20克,加入到100克水中充分溶解后,有固体剩余的是氯酸钾(填物质名称),要使这些剩余的固体物质继续溶解,可以采用的方法有升高温度或增加溶剂.
| 常见物质的溶解度(20℃) | ||||
| 物质名称 | 氯酸钾 | 硝酸钾 | 氯化钠 | 蔗糖 |
| 溶解度/克 | 7.4 | 31.6 | 36.0 | 203.9 |
8.为了区别O2与CO2两瓶无色气体,下列方法中不可行的是( )
| A. | 分别通入紫色石蕊溶液中 | B. | 用燃着的木条分别伸入瓶中 | ||
| C. | 分别通入澄清石灰水 | D. | 分别通入稀盐酸 |
9.某物质在空气中完全燃烧后,生成的气体能使澄清石灰水变浑浊,则该物质一定是( )
| A. | 碳单质 | B. | 含有碳元素、氢元素的化合物 | ||
| C. | 含有碳元素、氧元素的化合物 | D. | 含有碳元素的物质 |
 在自来水消毒过程中,通常要发生化学反应,其反应的微观过程可用如图表示:(图注:●表示氯原子○表示氧原子●表示氢原子)
在自来水消毒过程中,通常要发生化学反应,其反应的微观过程可用如图表示:(图注:●表示氯原子○表示氧原子●表示氢原子) 实验仪器的安全使用非常重要.
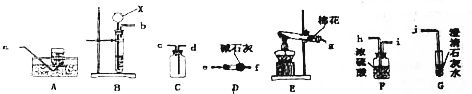
实验仪器的安全使用非常重要.