题目内容
1.课外小组的同学设计用氢氧化钠溶液来“捕捉”二氧化碳,其基本过程如下(部分条件及物质未标出).请回答下列有关问题: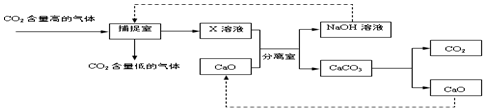
(1)“捕捉室”中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O;
(2)整个过程中没有涉及的基本化学反应类型是置换反应;
(3)在整个“捕捉”过程中,可以循环利用的物质是氧化钙、氢氧化钠 (填名称).
分析 (1)“捕捉室”中,氢氧化钠和二氧化碳反应生成碳酸钠和水;
(2)根据反应物、生成物的种类可以判断反应类型;
(3)根据“捕捉”过程可以判断循环利用的物质.
解答 解:(1)“捕捉室”中,氢氧化钠和二氧化碳反应生成碳酸钠和水,发生反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
故填:2NaOH+CO2=Na2CO3+H2O.
(2)整个过程中,氧化钙和水反应生成氢氧化钙,属于化合反应,碳酸钙分解生成氧化钙和二氧化碳,属于分解反应,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,属于复分解反应,没有涉及的基本化学反应类型是置换反应.
故填:置换反应.
(3)在整个“捕捉”过程中,可以循环利用的物质是氧化钙、氢氧化钠.
故填:氧化钙、氢氧化钠.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
15.如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( )


| A. | 10℃时,甲的溶解度小于乙的溶解度 | |
| B. | t℃时,甲、乙饱和溶液中溶质的质量分数一定相等 | |
| C. | 30℃时,将等质量的甲、乙配制成饱和溶液,加入水的质量甲小于乙 | |
| D. | 将甲、乙饱和溶液的温度从30℃降到10℃时,析出晶体的质量甲大于乙 |
16.下列对环境的有关说法中,错误的是( )
| A. | SO2、CO2、NO2的排放,是形成酸雨主要原因 | |
| B. | 白色污染是废弃塑料造成的污染 | |
| C. | 废水的任意排放是形成水污染的主要原因之一 | |
| D. | 烟尘、灰尘是形成雾霾的主要原因之一 |
9.下列叙述与对应的示意图表示正确的是( )
| A. |  加热一定质量的高锰酸钾制氧气 | |
| B. |  向等质量的不同金属中分别滴加足量的相同稀盐酸 | |
| C. |  向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液 | |
| D. |  向稀盐酸中滴加足量的水 |
16.下列有关水或溶液的说法正确的是( )
| A. | 用直流电电解水,发现负极与正极上得到的气体体积比约2:1 | |
| B. | 将FeCl3、蔗糖、汽油分别放入一定量的水中都能形成溶液 | |
| C. | 河水经过沉降、过滤、活性炭吸附后得到的水是纯净物 | |
| D. | 溶液一定是均一、稳定的液体 |
6.下列图象与对应选项关系合理的是( )
| A. |  向pH=13的氢氧化钠溶液中加水稀释 | |
| B. |  用相同质量的氯酸钾固体加热分解来制取氧气 | |
| C. |  向一定体积的氢氧化钠溶液中逐滴加入稀盐酸 | |
| D. |  向一定质量一定质量分数的稀盐酸中加入铁粉 |
