题目内容
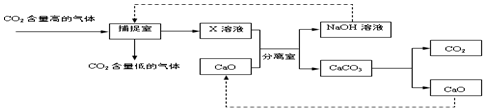
10.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并加以利用.用氢氧化钠溶液来“捕捉”CO2,其过程如下图所示(部分条件及物质未标出).(提示:高温反应炉中的反应为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)

请根据有关信息回答问题:
(1)用氢氧化钠溶液“捕捉”CO2的化学方程式为2NaOH+CO2=Na2CO3+H2O.
(2)反应分离室中需进行的实验操作为过滤.
(3)整个工业流程中,可以循环使用的物质是氢氧化钠和氧化钙.
分析 氢氧化钠能和二氧化碳反应生成碳酸钠和水,氧化钙能和水反应生成氢氧化钙,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,碳酸钙在高温条件下分解生成氧化钙和二氧化碳.
解答 解:(1)用氢氧化钠溶液“捕捉”二氧化碳时,氢氧化钠和二氧化碳反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O.
故填:2NaOH+CO2=Na2CO3+H2O.
(2)反应分离室中需进行的实验操作是过滤,通过过滤把碳酸钙从液体中分离出来.
故填:过滤.
(3)整个工业流程中,反应分离室中生成的氢氧化钠可以重新加入捕捉室进行再利用,碳酸钙分解生成的氧化钙进入反应分离室进行再利用,因此可以循环使用的物质是氢氧化钠和氧化钙.
故填:氢氧化钠和氧化钙.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
4.分析推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 中和反应有盐和水生成,所以生成盐和水的反应一定是中和反应 | |
| B. | 燃烧都伴随着发光、放热现象,所以有发光、放热现象的变化就是燃烧 | |
| C. | 碱性溶液能使酚酞试液变红,能使酚酞试液变红的溶液一定是碱溶液 | |
| D. | 化合物是由不同元素组成的纯净物,所以由不同元素组成的纯净物一定是化合物 |
18.某溶液中大量存在的离子今有NH4+、Ba2+和X离子,则X可能是( )
| A. | CO32- | B. | SO42- | C. | NO3- | D. | K+ |
5.下列实验操作中正确的是( )
| A. | 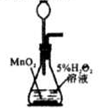 | B. | 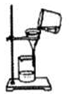 | C. |  | D. |  |
15.电影《从你的全世界路过》中陈末的一碗小面,再次勾起全国人民对重庆小面的喜爱之情.未进面馆,先闻面香,用分子的角度可以解释为( )
| A. | 分子可以再分 | B. | 分子在不断运动 | ||
| C. | 分子之间有间隔 | D. | 分子可以构成物质 |
2.空气成分中,体积分数约占78%的是( )
| A. | 稀有气体 | B. | 氧气 | C. | 氮气 | D. | 二氧化碳 |
19.“归纳与比较”是化学学习的主要方法.下列关于CO2与CO的比较正确的是( )
| A. | 组成:都是由碳和氧两种元素组成,但二氧化碳比一氧化碳多一个氧元素 | |
| B. | 性质:都能溶于水;CO能燃烧,而CO2不能燃烧 | |
| C. | 用途:干冰可用于人工降雨,CO可作气体燃料 | |
| D. | 危害:都有毒,CO2还会造成温室效应 |
20.生活和生产中,我们常根据需求会选择不同的去污或洗涤方法,下列去污或洗涤方式利用溶解原理的是( )
| A. | 医院用酒精除去工作服上的碘渍 | |
| B. | 钢管厂用盐酸清洗铁锈 | |
| C. | 厨房中用洗洁精清洗餐具上的油污 | |
| D. | 实验室用氢氧化钠溶液洗去氧气中混有的二氧化碳 |