题目内容
溶液是自然界中常见的物质.下列有关溶液的说法正确的是( )
A.溶液的上层浓度小,下层浓度大
B.溶液蒸干后,均能得到固体溶质
C.溶液中只有一种溶质时,溶液为纯净物
D.物质在溶解得到溶液的过程中,通常有放热或吸热的现象出现
【分析】A、根据溶液的均一性考虑;B、根据溶液中的溶质不一定是固体考虑;C、根据溶液中含有溶质和溶剂,一定是混合物考虑;D、根据物质溶解的两个过程考虑.
【解答】解:A、溶液具有均一性,液的上层浓度和下层浓度相同,故A错;
B、盐酸中的溶质是氯化氢气体,蒸干后不会有固体,故B错;
C、溶液中含有溶质和溶剂,一定是混合物,故C错;
D、物质在溶解得到溶液的过程中,构成物质的微粒向水中扩散的过程吸收热量,与水分子结合的过程放出热量,故D正确.
故选D.

同学们对制作糕点常用膨松剂Na2CO3或NaHCO3进行了下列探究.
【查阅资料】
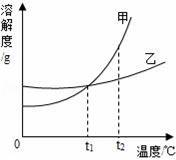
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
【探究一】NaHCO3和Na2CO3性质差异的探究
(1)现有20℃时溶质质量分数为8%的Na2CO3和NaHCO3溶液
酸碱性:取样于试管中,分别滴加紫色石蕊试液,均显 色;
酸碱度:NaHCO3溶液 Na2CO3溶液(填“>”或”“<”).
(2)稳定性:按图1,实验中可观察乙烧杯中的石灰水变浑浊,
甲烧杯不变,则乙烧杯中发生反应的化学方程式为: .
结论:在受热条件下,碳酸钠比碳酸氢钠稳定性 (填“强”或“弱”).
(3)利用溶解度鉴别NaHCO3和Na2CO3:分别取Xg两种固体粉末加入20℃,10g水中充分溶解,通过观察溶解现象来区分,X可以是下列的 .(选填A、B或C)
A.1.5g B.0.96g C.0.5g
【探究二】测定NaHCO3和Na2CO3混合物10.0g中NaHCO3的质量分数(图2,夹持装置略)
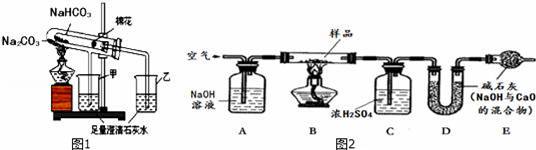

【问题讨论】
(4)实验前先通一段时间的空气的目的是 ;
(5)A的作用是 ,若没有装置E,NaHCO3的质量分数测定结果会 (填“偏大”、“不变”或“偏小”).
(6)停止加热后,仍继续通入空气一段时间,目的是 .
【含量测定】
(7)测得装置D的质量实验前为120.2g,实验后为122.4g,计算该样品中NaHCO3的质量分数.(要有计算过程)
【知识拓展】
(8)向Na2CO3溶液中通入CO2气体可以生成NaHCO3,该反应的化学反应方程式为: N .

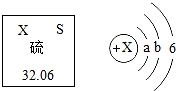

 CO2 B.2CO+O2
CO2 B.2CO+O2