题目内容
4.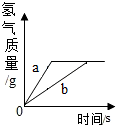 将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )| A. | a曲线表示锌 | B. | 反应消耗盐酸的总质量一定相等 | ||
| C. | 反应后盐酸一定没有剩余 | D. | 反应后锌一定有剩余 |
分析 A、根据活泼金属与酸反应的速率快进行分析;
B、由图可知生成的氢气质量是相等的,则参加反应的盐酸的质量也是相等的;
C、生成的氢气质量是相等的,则参加反应的盐酸的质量也是相等的;
D、生成的氢气质量相等,则消耗的盐酸质量相等,那么根据反应方程式可知铁消耗得少、锌消耗得多.
解答 解:A、锌比铁活泼,所以锌与酸反应的速率快,正确;
B、由图可知生成的氢气质量是相等的,则参加反应的盐酸的质量也是相等的,正确;
C、生成的氢气质量是相等的,则参加反应的盐酸的质量也是相等的,无剩余,正确;
D、如图最终生成的氢气质量相等,则消耗的盐酸质量相等,那么根据反应方程式可知铁消耗得少、锌消耗得多,已知根据“等质量的锌和铁”,因此铁一定有剩余,错误.
故选D.
点评 本题考查金属与酸反应的有关知识,综合性较强,不仅需要根据图象和题意分析出直接信息,还需要根据计算得出用量问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.雾霾是一种大气污染现象,不属于雾霾治理措施的是( )
| A. | 植树绿化,美化环境 | B. | 外出时佩戴防雾霾口罩 | ||
| C. | 提倡绿色出行,使用新能源汽车 | D. | 减少火力发电,增加太阳能发电 |
15.如图为某一反应的微观示意图,下列叙述正确的是( )


| A. | 反应前后各元素的化合价均不变 | |
| B. | 该反应为置换反应 | |
| C. | 该反应中含有2种氧化物 | |
| D. | 参加反应的两种物质的分子数比为1:1 |
19.报道中,科学家使用普通氧分子与带正电氧离子作用,制作出O4,下列关于O4的说法中,正确的是( )
| A. | O4与O2、与O3都是氧单质 | B. | O4属于化合物 | ||
| C. | O4分子是由氧元素构成的 | D. | 合成O4的反应属于化学变化 |
9. 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )| A. | 该元素原子的核外电子数为117 | B. | 该元素的原子序数为117 | ||
| C. | 该元素原子的中子为117 | D. | 钙和锫都属于金属元素 |
16.下列物质分类正确的是( )
| A. | 混合物:冰水、糖水 | B. | 氧化物:干冰、臭氧 | ||
| C. | 合成材料:涤纶、合金 | D. | 能导电:石墨、硬铝 |
14.下列是今年无锡市实验操作考查“药品的取用和加热”中部分实验操作示意图.其中正确的是( )
| A. |  用纸槽将固体粉末送入试管 | B. |  倾倒液体 | ||
| C. |  加热试管内液体 | D. |  熄灭酒精灯 |
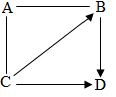 A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).
A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去). 根据给出的元素周期表中部分原子的结构示意图,回答问题.
根据给出的元素周期表中部分原子的结构示意图,回答问题. ,推测氧元素在元素周期表中应排在第二周期.
,推测氧元素在元素周期表中应排在第二周期.