题目内容
12.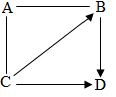 A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).
A、B、C、D为初中常见的物质,相互之间的关系如图所示(“-”表示两种物质间能发生反应,“→”表示两种物质间能够转化,部分反应物或生成物以及反应条件已略去).(1)若A是一种能供给呼吸的气体单质,气体B能用于炼铁,C是一种黑色固体单质且具有吸附性.则:
①A的化学式是O2;
②C→D反应的化学方程式是C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2(合理即可).
(2)若A是一种碱,B被广泛应用于玻璃、造纸、纺织和洗涤剂的生产,C是非金属氧化物,其固态时能进行人工降雨.则:
①B的化学式是Na2CO3;
②固体C的俗名为干冰;
③B→D反应的化学方程式是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH(或其它合理答案).
分析 (1)A是一种能供给呼吸的气体单质,气体B能用于炼铁,C是一种黑色固体单质且具有吸附性,因此A是氧气,C是碳,则B为一氧化碳;一氧化碳和碳都能产生D,因此D是二氧化碳;
(2)A是一种碱,B被广泛应用于玻璃、造纸、纺织和洗涤剂的生产,C是非金属氧化物,其固态时能进行人工降雨,因此C是二氧化碳,A和B能够反应,因此A是氢氧化钙,B是碳酸钠;碳酸钠和二氧化碳都能反应产生D,因此D可以是碳酸钙,据此分析.
解答 解:(1)A是一种能供给呼吸的气体单质,气体B能用于炼铁,C是一种黑色固体单质且具有吸附性,因此A是氧气,C是碳,则B为一氧化碳;一氧化碳和碳都能产生D,因此D是二氧化碳;碳和氧气点燃产生二氧化碳;
故答案为:O2; C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 (合理即可);
(2)A是一种碱,B被广泛应用于玻璃、造纸、纺织和洗涤剂的生产,C是非金属氧化物,其固态时能进行人工降雨,因此C是二氧化碳,俗名干冰;A和B能够反应,氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠,因此A是氢氧化钙,B是碳酸钠;碳酸钠和二氧化碳都能反应产生D,因此D可以是碳酸钙,①Na2CO3 ②干冰 ③Ca(OH)2+Na2CO3=CaCO3↓+2NaOH(或其它合理答案).
点评 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺藤摸瓜顺向、逆向或两边向中间推,逐一导出其他结论.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
2. 如图所示,打开分液漏斗的旋塞,滴下少量双氧水.下列现象正确的是( )
如图所示,打开分液漏斗的旋塞,滴下少量双氧水.下列现象正确的是( )
 如图所示,打开分液漏斗的旋塞,滴下少量双氧水.下列现象正确的是( )
如图所示,打开分液漏斗的旋塞,滴下少量双氧水.下列现象正确的是( )| A. | 气球涨大,红墨水左移 | B. | 气球缩小,红墨水右移 | ||
| C. | 气球涨大,红墨水右移 | D. | 气球缩小,红墨水左移 |
3.在一个密闭容器中放人甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应结束后,测得部分数据如表.下列说法中,正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X | 26 | 2 | 12 |
| A. | 乙是反应物 | B. | 无法确定X的值 | ||
| C. | 该反应可能是复分解反应 | D. | 物质丙可能是该反应的催化剂 |
20.下列化学用语书写正确的是( )
| A. | 硫酸钾:KSO4 | B. | 钙离子:Ca+2 | ||
| C. | 2个氮原子:N2 | D. | 显+2价的镁元素:$\stackrel{+2}{Mg}$ |
7.饮食健康是人民群众普遍的生活需求.下列说法不正确的是( )
| A. | 适量的小苏打用于制作面包 | |
| B. | 蛋白质的摄入可促进肌肉的修补 | |
| C. | 奶茶中添加塑化剂使其口感更加香醇 | |
| D. | 酱油中添加铁元素可预防缺铁性贫血 |
17.实验设计是化学实验的重要环节,请根据下列实验要求回答相关问题:
【活动与探究一】用对比实验方法探究二氧化碳的性质.
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”) 瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)实验二观察到C装置中发生的现象是湿润的蓝色石蕊试纸变红,而干燥的不变,结论是CO2与水反应变成碳酸,碳酸能使紫色石蕊试纸变红(用语言表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
(3)实验三目的是探究温度对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响.
【活动与探究一】用对比实验方法探究二氧化碳的性质.
| 实验一 | 实验二 |
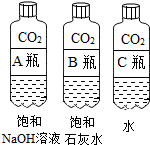 |  |
(2)实验二观察到C装置中发生的现象是湿润的蓝色石蕊试纸变红,而干燥的不变,结论是CO2与水反应变成碳酸,碳酸能使紫色石蕊试纸变红(用语言表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
| 实验三 | 实验四 |
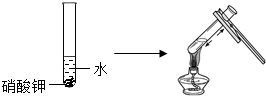 | 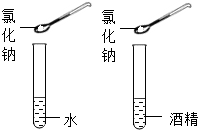 |
4.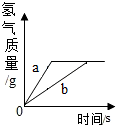 将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
 将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )| A. | a曲线表示锌 | B. | 反应消耗盐酸的总质量一定相等 | ||
| C. | 反应后盐酸一定没有剩余 | D. | 反应后锌一定有剩余 |
 、H-O-、-O-O-”等几种,你认为青蒿素分子中起杀菌作用的原子间相互结合的方式是-O-O-.以上是运用已有知识进行的推理,推理是否正确,需要通过实验进行验证.
、H-O-、-O-O-”等几种,你认为青蒿素分子中起杀菌作用的原子间相互结合的方式是-O-O-.以上是运用已有知识进行的推理,推理是否正确,需要通过实验进行验证.