题目内容
9. 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )| A. | 该元素原子的核外电子数为117 | B. | 该元素的原子序数为117 | ||
| C. | 该元素原子的中子为117 | D. | 钙和锫都属于金属元素 |
分析 根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
解答 解:A.由上图知,该元素的原子序数为117,根据原子序数=质子数=核外电子数,所以该元素的核外电子数为117,故说法正确;
B.由上图知,该元素的原子序数为117,故说法正确;
C.由上图知,117是该元素的原子序数,即核电荷数、质子数而不是中子数,故说法错误;
D.根据钙和锫元素的汉语名称的偏旁为金字旁可知,都属于金属元素,故说法正确;
故选C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法等进行分析解题的能力.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
19.生活中的下列做法不正确的是( )
| A. | 用食醋除去暖水瓶中的水垢 | |
| B. | 用燃烧的方法鉴别衣料中的羊毛纤维 | |
| C. | 儿童患佝偻病是因为体内缺乏微量元素碘 | |
| D. | CO(NH2)2(尿素)、(NH4)2SO4和NaNO3均可用作氮肥 |
20.下列化学用语书写正确的是( )
| A. | 硫酸钾:KSO4 | B. | 钙离子:Ca+2 | ||
| C. | 2个氮原子:N2 | D. | 显+2价的镁元素:$\stackrel{+2}{Mg}$ |
17.实验设计是化学实验的重要环节,请根据下列实验要求回答相关问题:
【活动与探究一】用对比实验方法探究二氧化碳的性质.
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”) 瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)实验二观察到C装置中发生的现象是湿润的蓝色石蕊试纸变红,而干燥的不变,结论是CO2与水反应变成碳酸,碳酸能使紫色石蕊试纸变红(用语言表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
(3)实验三目的是探究温度对硝酸钾溶解性的影响;实验四是探究溶剂种类对物质溶解性的影响.
【活动与探究一】用对比实验方法探究二氧化碳的性质.
| 实验一 | 实验二 |
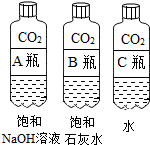 |  |
(2)实验二观察到C装置中发生的现象是湿润的蓝色石蕊试纸变红,而干燥的不变,结论是CO2与水反应变成碳酸,碳酸能使紫色石蕊试纸变红(用语言表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
| 实验三 | 实验四 |
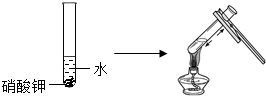 | 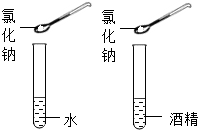 |
4.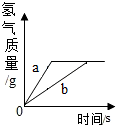 将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
 将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
将等质量的锌和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )| A. | a曲线表示锌 | B. | 反应消耗盐酸的总质量一定相等 | ||
| C. | 反应后盐酸一定没有剩余 | D. | 反应后锌一定有剩余 |
14.关于水的说法正确的是( )
| A. | 水是人体必需的营养素之一 | B. | 可用煮沸方法检验软水和硬水 | ||
| C. | 生活污水可直接排放到江河中 | D. | 电解水时电源负极产生氧气 |
18.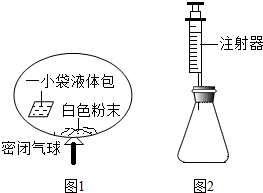 某研究小组对自动充气气球(示意图如图1)进行下列探究.
某研究小组对自动充气气球(示意图如图1)进行下列探究.
[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为检验气体是二氧化碳,可选用氢氧化钙溶液(填试剂名称).
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈酸性.
探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠.
[设计并进行实验]
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确(填“正确”或“不正确”).
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
实验①的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;表中a=0.1;V1>V2(填“>”、“<”或“=”).
[分析并得出结论]
(5)如何从上表中获取证据并得出结论?根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
 某研究小组对自动充气气球(示意图如图1)进行下列探究.
某研究小组对自动充气气球(示意图如图1)进行下列探究.[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为检验气体是二氧化碳,可选用氢氧化钙溶液(填试剂名称).
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈酸性.
探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠.
[设计并进行实验]
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确(填“正确”或“不正确”).
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
| 实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
| 名称 | 质量/g | ||
| ① | 碳酸氢钠 | 0.10 | V1 |
| ② | 碳酸钠 | 0.10 | V2 |
| ③ | 白色粉末 | a | V1 |
[分析并得出结论]
(5)如何从上表中获取证据并得出结论?根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
19.只用下列鉴别方法不能把待鉴别物质区分开的是( )
| 选项 | 待鉴别物质 | 鉴别方法 |
| A | 软水、硬水 | 分别滴加肥皂水,搅拌,观察产生泡沫多少 |
| B | 棉纤维、羊毛纤维 | 分别点燃,闻燃烧产生的气味 |
| C | 氯化钠溶液、稀盐酸 | 分别滴加酚酞溶液,观察溶液颜色变化 |
| D | 氯化钾溶液、硫酸钠溶液 | 分别滴加氢氧化钡溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |