题目内容
10.一水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸反应(假设石灰石样品中的杂质不与稀盐酸反应,也不溶于水).有关实验数据如表.| 实验数据 | 反应前 | 反应后 | |
| 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和反应后混合物的质量 | |
| 300g | 24g | 315.2g | |
(2)石灰石样品中碳酸钙的质量是多少?
(3)该石灰石矿石中碳酸钙的质量分数是多少(计算结果精确到0.1%)?
分析 (1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中碳酸钙的质量分数.
解答 解:(1)根据质量守恒定律,二氧化碳的质量为:300g+24g-315.2g=8.8g;
(2)设该石灰石样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
此石灰石中碳酸钙的质量分数为:$\frac{20g}{24g}$×100%≈83.3%.
故答案为:(1)8.8g;
(2)20g;
(3)83.3%.
点评 本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | “绿色食品”都是绿色的植物 | |
| B. | 植物的光合作用有益于生态平衡 | |
| C. | 吸烟会危害人体健康,但不会污染环境 | |
| D. | 发电厂热水直接排入江河,有利于鱼类生存 |
15.如表是某城市某日空气质量报告:
某研究性学习小组对表中首要污染物S02:导致酸雨的成因进行探究.
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.
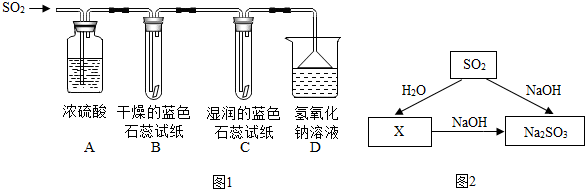
(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | S02 | Ⅱ | 良 |
(提示:S02:是一种无色、有刺激性气味的有毒气体,易溶于水,具有与C02相似的化学性质)
【探究实验】实验一:用如图1所示装置进行实验.

(1)A装置的作用是干燥 SO2气体.
(2)实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变红色,说明SO2与水反应生成一种酸.
(3)D装置的作用是吸收SO2,防止污染空气,发生反应的化学方程式是SO2+2NaOH═Na2SO3+H2O.
实验二:往盛有水的烧杯中通人SO2气体,测所得溶液的pH< 7(填“>”“=”或“<”),然后每隔l小时测定其pH,发现pH逐渐变小,直至恒定,说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4.
【查阅资料】SO2形成酸雨的另一途径:S02与空气中的02在飘尘的作用下反应生成SO3
(飘尘的质量和性质在反应前后不发生变化),SO3溶于降水生成H2SO4.在此过程中飘尘作催化剂.
【探究结论】SO2与空气中的氧气、水反应生成硫酸而形成酸雨.该市可能易出现酸雨.
【模拟实验】(1)由于食醋和酸雨的酸度(pH)差不多,
因此酸雨对大理石的作用可以通过大理石碎片放在醋中来模拟.当把2.0g大理石碎片放在醋中一整夜后,取出固体干燥称重,其质量可能是(醋酸钙易溶于水)A.
A.小于2.0gB.正好2.0g C.大于2.0g
(2)这组学生还做了另一个实验,即将大理石碎片放在蒸馏水中过夜,
其实验的目的是作对照,证明对大理石起腐蚀作用的是醋酸而不是水
【知识联想】SO2具有与CO2相似的化学性质,
根据图2给出的SO2及其化合物问的相互转化关系回答:
X的化学式是H2SO3,
写出X与NaOH反应的化学方程H2SO3+2NaOH═Na2SO3+2H2O.
2.我市某日的空气质量日报如下表.下列说法不正确的是( )
| 项目 | 空气污染指数 | 空气质量级别 | 空气质量 |
| 可吸入颗粒 | 65 | Ⅱ | 良 |
| 二氧化硫 | 10 | ||
| 二氧化氮 | 20 |
| A. | 空气质量级别越高,空气质量状况越差 | |
| B. | 露天焚烧垃圾可加剧以上三个项目的污染指数 | |
| C. | 造成空气污染的主要气体是NO2、SO2、CO等 | |
| D. | 可吸入颗粒就是PM2.5 |
 如图为实验室制取二氧化碳的实验装置图,请回答下列问题:
如图为实验室制取二氧化碳的实验装置图,请回答下列问题: