题目内容
19.高锰酸钾受热分解:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(分解反应)分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应符合“一变多”的特征,属于分解反应.
故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
相关题目
9.下列物质的认识正确的是( )
| A. | 某专家称能“水变油”“点石成金” | |
| B. | 吸烟对青少年生长发育无害 | |
| C. | 生活中使用天然气做饭要通风透气 | |
| D. | 被毒鼠强药死的鸭水,煮熟后可以食用 |
10.一水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸反应(假设石灰石样品中的杂质不与稀盐酸反应,也不溶于水).有关实验数据如表.
(1)反应中生成二氧化碳的质量为8.8g.
(2)石灰石样品中碳酸钙的质量是多少?
(3)该石灰石矿石中碳酸钙的质量分数是多少(计算结果精确到0.1%)?
| 实验数据 | 反应前 | 反应后 | |
| 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和反应后混合物的质量 | |
| 300g | 24g | 315.2g | |
(2)石灰石样品中碳酸钙的质量是多少?
(3)该石灰石矿石中碳酸钙的质量分数是多少(计算结果精确到0.1%)?
7.建立宏观与微观的联系是化学独特的思维方式,下列对宏观现象的微观解释不正确的是( )
| A. | 水和过氧化氢的化学性质不同,是因为这两种物质的分子构成不同 | |
| B. | CO2使紫色石蕊试液变红,是因为CO2分子能与紫色石蕊发生化学反应 | |
| C. | 哇哈哈富氧水能够补氧,是因为富氧水里溶有氧气分子 | |
| D. | 高山上喝空的矿泉水瓶,抒紧瓶盖,下山后瓶子变瘪,是因为瓶内的气体分子变小 |
14.某物质在隔绝空气加强热时生成的二氧化碳和水,则此物质的组成叙述正确的是( )
| A. | 一定含碳、氢、氧三种元素 | B. | 一定只含氧元素 | ||
| C. | 一定含碳元素和氢元素 | D. | 一定不含氧元素 |
4.毕倭寇同学想通过实验,探究某企业用氨碱法生产纯碱样品的成分及含量.
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,毕倭寇同学做出如下假设:(1)只含有Na2CO3;(2)含有Na2CO3和 NaHCO3【查阅资料】
(1)表中的现象I为产生气泡;
(2)现象Ⅱ对应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验探究】为了确定纯碱样品的成分,毕倭寇同学设计如下实验方案,请你一起完成下列实验报告.
【实验反思】实验步骤A中,氯化钙溶液过量的目的是将碳酸钠全部除去.
【提出问题2】如何测量该纯碱样品中各物质的含量?
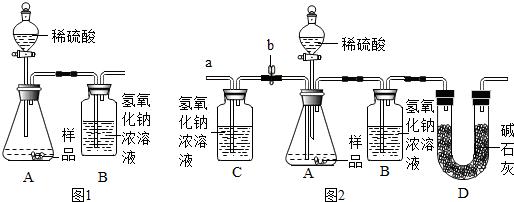
(1)为测量该纯碱样品各成分的含量,毕倭寇同学设了图1装置,通过称量B装置中质量变化来确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①空气中的CO2进入装置B被氢氧化钠吸收;②装置A中残留的CO2未被装置B中的氢氧化钠吸收.
(2)毕倭寇同学在老师的指导下重新设计了如图2所示的实验装置.该实验有以下操作步骤:
①查装置气密性,将Wg干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是①③②④⑥⑤⑦.
【提出问题】该纯碱样品中含有哪些物质?
【猜想与假设】通过分析,毕倭寇同学做出如下假设:(1)只含有Na2CO3;(2)含有Na2CO3和 NaHCO3【查阅资料】
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象I | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
(2)现象Ⅱ对应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验探究】为了确定纯碱样品的成分,毕倭寇同学设计如下实验方案,请你一起完成下列实验报告.
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| A取少量样品溶于水,加入过量的CaCl2溶液 | ①有白色沉淀产生 | 该反应的方程式:②Na2CO3+CaCl2═CaCO3↓+2NaCl |
| B将上述反应后的混合液过滤,取滤液③滴加稀盐酸 | ④有气泡冒出 | 证明猜想②成立 |

【实验反思】实验步骤A中,氯化钙溶液过量的目的是将碳酸钠全部除去.
【提出问题2】如何测量该纯碱样品中各物质的含量?
(1)为测量该纯碱样品各成分的含量,毕倭寇同学设了图1装置,通过称量B装置中质量变化来确定样品中各成分的含量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误,但多次实验发现,测定结果有偏差.造成偏差的原因有①空气中的CO2进入装置B被氢氧化钠吸收;②装置A中残留的CO2未被装置B中的氢氧化钠吸收.
(2)毕倭寇同学在老师的指导下重新设计了如图2所示的实验装置.该实验有以下操作步骤:
①查装置气密性,将Wg干燥的样品放入锥形瓶中;
②称量盛有氢氧化钠浓溶液的B瓶质量;
③打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤再次称量盛有氢氧化钠浓溶液的B瓶质量;
⑥打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
⑦根据B瓶增加的质量,计算样品中各成分的含量.
该实验的正确步骤是①③②④⑥⑤⑦.
11.如图所示的实验操作正确的是( )
| A. |  实验室制取二氧化碳 | B. |  盖灭酒精灯 | ||
| C. |  实验室制取氧气 | D. |  过滤 |
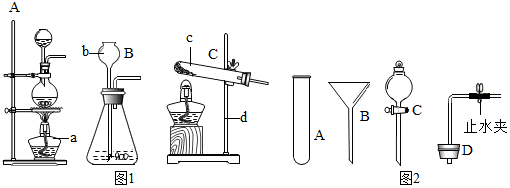
 淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状提出问题,并在实验室进行了以下探究.
淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状提出问题,并在实验室进行了以下探究.