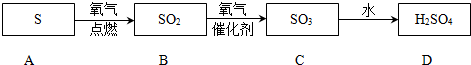
题目内容
7.根据下列装置图回答问题: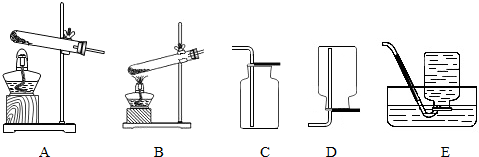
(1)某同学用氯酸钾和二氧化锰共热制备和收集氧气,他应选用的气体发生装置是A(填序号),选择依据是反应物是固体,反应需要加热.选用装置E来收集氧气,其原因氧气不易溶于水,该反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)A装置试管口向下倾斜的目的防止冷凝水回流炸裂试管.若选用C收集氧气,你认为验满的方法是把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满
(3)实验结束拆除装置后,发现试管炸裂,试分析造成此后果的可能原因没有预热,试管触及灯芯(要求答出2点即可).
(4)在实验开始时,称得固体总质量为30g,反应一段时间后,再次称量固体质量为25.2g,请计算实验过程中共消耗氯酸钾的质量.
分析 (1)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
氧气的密度比空气的密度大,不易溶于水;
(2)为了防止冷凝水回流时炸裂试管,试管口应该略向下倾斜;
氧气能够支持燃烧,能使带火星的木条复燃;
(3)如果操作不当,会影响实验结果,甚至会导致实验失败;
(4)反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算反应的氯酸钾的质量.
解答 解:(1)用氯酸钾和二氧化锰制备氧气需要加热,应选用的气体发生装置是A,选择依据是:反应物是固体,反应需要加热;
选用装置E来收集氧气,其原因是氧气不易溶于水,该反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
故填:A;反应物是固体,反应需要加热;氧气不易溶于水;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)A装置试管口向下倾斜的目的是防止冷凝水回流炸裂试管;
若选用C收集氧气,验满的方法是:把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
故填:防止冷凝水回流炸裂试管;把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(3)如果没有预热,加热时试管外壁有水,试管触及灯芯,实验结束拆除装置时先熄灭酒精灯等,都能够导致试管炸裂.
故填:没有预热,试管触及灯芯.
(4)设反应的氯酸钾的质量为x,
反应生成氧气的质量为:30g-25.2g=4.8g,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$,
x=12.25g,
答:反应的氯酸钾质量是12.25g.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 水 | B. | 氧气 | C. | 可燃物 | D. | 温度达到着火点 |
| A. | 水电解生成氢气和氧气--分子能够再分 | |
| B. | 打开试卷,能闻到油墨的味道--分子在不断的运动 | |
| C. | 物体的热胀冷缩--分子的体积大小发生了变化 | |
| D. | 气体能被压缩--分子之间有间隔 |
| 药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
| 药品 | 铜、锌 | 红磷、硫 | 氢氧化钠、氢氧化钙 | 盐酸、硫酸 |
| A. | 甲柜 | B. | 乙柜 | C. | 丙柜 | D. | 丁柜 |
 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系: 实验室制取氧气的装置如图所示.
实验室制取氧气的装置如图所示.  按如图连接好装置图,打开止水夹a在乙中产生的现象是导管下端产生气泡;,反应片刻后夹紧止水夹a,此时乙中出现的现象是出现白色沉淀,写出乙中反应的化学方程式AlCl3+3AgNO3=Al(NO3)3+3 AgCl↓ 或 HCl+AgNO3=HNO3+AgCl↓.
按如图连接好装置图,打开止水夹a在乙中产生的现象是导管下端产生气泡;,反应片刻后夹紧止水夹a,此时乙中出现的现象是出现白色沉淀,写出乙中反应的化学方程式AlCl3+3AgNO3=Al(NO3)3+3 AgCl↓ 或 HCl+AgNO3=HNO3+AgCl↓. 如图所示,依据A、B、C三种固体物质的溶解度曲线.回答下列问题:
如图所示,依据A、B、C三种固体物质的溶解度曲线.回答下列问题: