题目内容
3.乙醇燃烧乙成为国际上普遍公认可降低环境污染和取代化石燃料的主要资源.某研究性学习小组为了探究乙醇在氧气中燃烧的产物,将乙醇在一定量的氧气中点燃,再将燃烧后的混合气体通过如下的装置进行实验.请填空: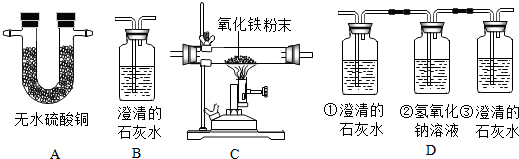
(1)为尽可能多地检验出乙醇的燃烧产物,如图所示装置的正确连接顺序为:混合气体→A→D→C→B(填写装置序号,装置不重复使用).
(2)该学习小组的同学通过正确的设计并进行实验,在实验过程中观察到的部分现象为:A装置中的白色固体变蓝、B和D中①装置内的澄清石灰水均变浑浊,而D中③装置内的澄清石灰水不变浑浊,根据实验结果并通过分析推理,得出这次实验中乙醇的燃烧产物为CO、CO2、H2O(填写化学式).
(3)如果将D中②、③装置去掉,则可能会影响对燃烧产物中CO的检验.
(4)依据这次实验中乙醇的燃烧产物,请说明你对乙醇组成的判断:乙醇中含有碳、氢、氧三种元素.
分析 (1)根据乙醇含有的元素,结合质量守恒定律来解答;
(2)根据实验现象来判断乙醇燃烧的产物.二氧化碳能使澄清的石灰水变浑浊,一氧化碳具有还原性,无水硫酸铜遇水变成蓝色;
(3)根据二氧化碳的检验方法分析;
(4)根据实验结果分析判断.
解答 解:(1)乙醇中含有碳元素、氢元素和氧元素,在燃烧时可能产生一氧化碳、二氧化碳和水等物质,检验一氧化碳可以用氧化铜,检验二氧化碳可以用澄清石灰水,检验水常用无水硫酸铜,考虑到一氧化碳能够反应生成二氧化碳,所以应该先检验二氧化碳,然后检验一氧化碳,而气体通过澄清石灰水时会带出水蒸气,故应该最先检验水,然后是二氧化碳,最后检验一氧化碳;所以顺序是:混合气体→C→A→B→D;
(2)根据A中①装置内的澄清石灰水均变浑浊,而A中③装置内的澄清石灰水不变浑浊,D中石灰水变浑浊可知生成了一氧化碳,故可以知道乙醇燃烧后的产物为一氧化碳、二氧化碳和水;
(3)由于二氧化碳能使澄清的石灰水变浑浊,如果将A中①装置是用来检验二氧化碳,②装置是用来除去多余的二氧化碳,③装置是用来检验二氧化碳是否已除尽,②和③的目的是为了对后续CO的检验不产生干扰,因此如果将A中②、③装置去掉,则不能验证产物中的CO.
(4)依据这次实验中乙醇的燃烧产物,根据质量守恒定律,乙醇中含有碳、氢、氧三种元素:
故答为:(1)A→D→C;(2)CO、CO2、H2O;(3)CO:(4)乙醇中含有碳、氢、氧三种元素.
点评 熟练掌握质量守恒定律的实质,能够根据质量守恒定律来判断反应后生成的物质,知道影响物质燃烧的剧烈程度的因素.

练习册系列答案
相关题目
14.研究表明,氨气在一定条件下能与氧气发生反应,其主要化学反应为:4NH3+3O2$\frac{\underline{\;一定条件\;}}{\;}$2X+6H2O,则X的化学式是( )
| A. | NO | B. | N2 | C. | NO2 | D. | N2O |
11.下列物质的化学名称与俗名,对应错误的是( )
| A. | 氧化钙--熟石灰、消石灰 | B. | 汞--水银 | ||
| C. | 碳酸氢钠--小苏打 | D. | 氢氧化钠--烧碱、火碱、苛性钠 |
18.在已调节至平衡的托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸;然后向左、右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是(酸的挥发忽略不计)( )
| A. | 10g碳酸钙和10g碳酸钠 | B. | 10g碳酸钙和5.6g硝酸银 | ||
| C. | 5.6g铁粉和5.6g锌粉 | D. | 2.4g镁和2.2g氧化镁 |
8.四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如图所示,则有关说法中正确的是( )


| A. | 甲一定是化合物 | B. | 乙一定是这个反应的催化剂 | ||
| C. | 该反应属于分解反应 | D. | 丙可能是反应物 |
13. 槐安大桥是石家庄第一座斜拉大桥(如图所示),大桥的建设及通行涉及到许多理化知识,下列说法中不正确的是( )
槐安大桥是石家庄第一座斜拉大桥(如图所示),大桥的建设及通行涉及到许多理化知识,下列说法中不正确的是( )
 槐安大桥是石家庄第一座斜拉大桥(如图所示),大桥的建设及通行涉及到许多理化知识,下列说法中不正确的是( )
槐安大桥是石家庄第一座斜拉大桥(如图所示),大桥的建设及通行涉及到许多理化知识,下列说法中不正确的是( )| A. | 大桥建设中桥墩的地基很宽大,是为了减小压强 | |
| B. | 大桥建设过程中使用了大量的钢,其硬度小于纯铁的硬度 | |
| C. | 采用多根斜拉索的目的是让每根斜拉索所受的拉力减小 | |
| D. | 大桥钢铁器件喷上油漆是为防止铁与空气中的氧气和水反应而生锈 |

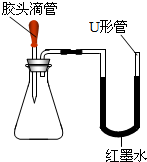 如图是某同学设计的趣味实验装置,其气密性良好.
如图是某同学设计的趣味实验装置,其气密性良好.