题目内容
18.在已调节至平衡的托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸;然后向左、右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是(酸的挥发忽略不计)( )| A. | 10g碳酸钙和10g碳酸钠 | B. | 10g碳酸钙和5.6g硝酸银 | ||
| C. | 5.6g铁粉和5.6g锌粉 | D. | 2.4g镁和2.2g氧化镁 |
分析 因为加入的盐酸质量相等,所以需要判断两端加入一定量物质后增加质量是否相等,增加质量相等时天平能仍然保持平衡,不相等时天平发生偏转.可根据化学方程式,借助关系式和差量法进行分析比较.
解答 解:50g 7.3%的稀盐酸中HCl质量=50g×7.3%=3.65g
A、CaCO3+2HCl=CaCl2+H2O+CO2↑ Na2CO3+2HCl=2NaCl+H2O+CO2↑
100 73 106 73
由化学方程式可知,碳酸钠、碳酸钙过量,所以依据盐酸可以求出生成的二氧化碳质量相等,所以反应后烧杯中中增加质量相等,天平平衡,故不正确;
B、硝酸银与盐酸反应不产生气体,因此增加的质量即为加入的硝酸银溶液质量5.6g;
而CaCO3与盐酸反应放出气体二氧化碳,
CaCO3 ~CO2
100 44
10g m(CO2)
$\frac{100}{10g}=\frac{44}{m(C{O}_{2})}$
解之得 m(CO2)=4.4g
所以加碳酸钙后烧杯质量增加质量为10g-4.4=5.6g,所以天平仍然平衡.故不正确;
C、50g 7.3%的稀盐酸完全反应消耗金属铁和锌的质量分别为:
Fe~2HCl
56 73
m(Fe) 3.65g
$\frac{56}{m}=\frac{73}{3.65g}$
解之得 m(Fe)=2.8g
Zn~2HCl
65 73
m(Zn)3.65g
$\frac{65}{m}=\frac{73}{3.65g}$
解之得 m(Zn)=3.25g
则金属铁、锌均与稀盐酸没有反应完,盐酸少量,反应放出氢气质量相等;加入金属质量相等,天平平衡;故不正确;
D、50g 7.3%的稀盐酸完全反应消耗金属镁的质量为x,生成氢气的质量为y
Mg~2HCl~H2
24 73 2
x 3.65g y
$\frac{24}{x}=\frac{73}{3.65g}$
x=1.2g
生成氢气的质量为$\frac{73}{3.65g}=\frac{2}{y}$
y=0.1g
镁过量,烧杯质量增加了2.4g-0.1=2.3g
而氧化镁和盐酸反应不放出气体,所以增加2.2g,所以天平不平衡.故正确.
答案:D
点评 加入物质充分反应后,天平一端增加的质量=加入固体质量-放出气体的质量,只有加入物质与放出气体质量均相等时,天平才能保持平衡.由于运算量比较大,所以对于有关化学方程式的计算是否熟练是解题的关键.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案| A. | 在含砂粒较多、潮湿、透气的土壤中 | B. | 在干燥、致密、透气的土壤中 | ||
| C. | 在潮湿、疏松、透气的土壤中 | D. | 在呈酸性的潮湿土壤中 |

| A. | 大量燃烧煤易导致酸雨 | |
| B. | 天然气是一种石油加工产品 | |
| C. | 家用燃料更新的理由之一是便于管道输送 | |
| D. | 气态燃料与空气接触充分,可提高燃料利用率 |
 化学就在我们身边.
化学就在我们身边.
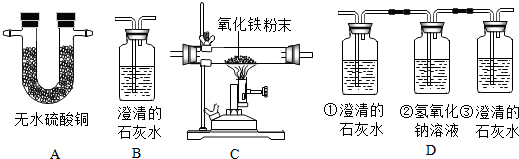
 如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.
如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.