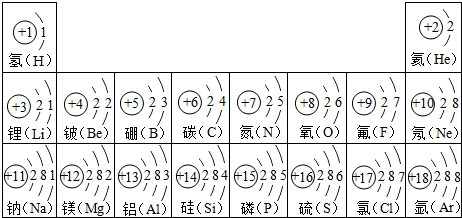
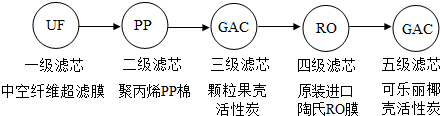
题目内容
12.为测定某铜锌合金中锌的含量,某同学称取了10.0g该合金放入盛有40.0g稀硫酸(H2SO4)的烧杯中.恰好完全反应,称得烧杯内物质的总质量为49.8g.试计算:
(1)生成氢气的质量为:0.2 g;
(2)该合金中锌的质量分数.
分析 根据反应的化学方程式进行计算,铁和铜加入稀硫酸中只有锌和稀硫酸反应,总质量减少的量就是生成的氢气的质量.
解答 解:(1)反应后产生的氢气质量为:10.0g+40.0g-49.8g=0.2g;故答案为:0.2;
(2)解:设Zn的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{x}=\frac{2}{0.2g}$
x=6.5g
该合金中锌的质量分数=$\frac{6.5g}{10.0g}$×100%=65.0%.
答:该合金中锌的质量分数65.0%.
点评 本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式进行.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 焊锡的熔点高于锡的熔点 | |
| B. | 相同情况下,同样大小的滤纸片比乒乓球片更容易燃烧 | |
| C. | 稀土是储量较少的一类金属的统称,属于不可再生资源 | |
| D. | 工业上利用液态氮气和液态氧气的密度不同制取氧气 |
1.某学习小组对硫酸进行如下研究:
(1)若对稀硫酸进行如下操作,溶液的pH升高的有ABC(填字母).
A、加少量水 B、加少量铁粉
C、加少量氢氧化钾 D、加少量浓硫酸
(2)向两个烧杯中分别注入两种硫酸,甲(溶质质量分数为98%,密度为1.84g/cm3)和乙(硫酸钾与水的暗体积比1:1混合)各10ml,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见表:
①若量取硫酸甲时俯视读数,在其他操作正确的情况下,所配硫酸乙的溶质质量分数将偏小(填“偏大”、“偏小”或“内能”).
②由表中实验数据可知:有关硫酸吸水性的说法错误的是B(填字母).
A、硫酸甲和乙都有吸水性 B、只有硫酸甲有吸水性 C、硫酸甲的吸水性较硫酸乙强
(3)小军同学利用稀释后的稀硫酸和硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中发生中和反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O;
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液,经测定,该溶液显酸性,则在该溶液中一定含有的离子是H+、Na+、K+和NO3-,可能含有的离子是Ba2+或SO42-.
(1)若对稀硫酸进行如下操作,溶液的pH升高的有ABC(填字母).
A、加少量水 B、加少量铁粉
C、加少量氢氧化钾 D、加少量浓硫酸
(2)向两个烧杯中分别注入两种硫酸,甲(溶质质量分数为98%,密度为1.84g/cm3)和乙(硫酸钾与水的暗体积比1:1混合)各10ml,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见表:
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
②由表中实验数据可知:有关硫酸吸水性的说法错误的是B(填字母).
A、硫酸甲和乙都有吸水性 B、只有硫酸甲有吸水性 C、硫酸甲的吸水性较硫酸乙强
(3)小军同学利用稀释后的稀硫酸和硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中发生中和反应的化学方程式H2SO4+2NaOH═Na2SO4+2H2O;
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液,经测定,该溶液显酸性,则在该溶液中一定含有的离子是H+、Na+、K+和NO3-,可能含有的离子是Ba2+或SO42-.
 已知A、B、C、D四种物质中含有相同的金属元素,A为红棕色固体.C、D中含元素种类相同,E与C、D属于同一类另的物质,B→A反应过程较为复杂.“→”表示一种物质转化成另一种物质,五种物质的转化关系如下:(1)C物质的化学式是FeCl3.
已知A、B、C、D四种物质中含有相同的金属元素,A为红棕色固体.C、D中含元素种类相同,E与C、D属于同一类另的物质,B→A反应过程较为复杂.“→”表示一种物质转化成另一种物质,五种物质的转化关系如下:(1)C物质的化学式是FeCl3.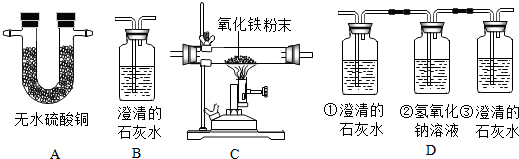
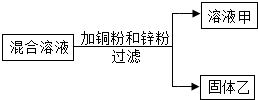 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,现有下列说法:
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,现有下列说法: