题目内容
16.化学对社会发展的重要贡献之一,就是不断研发新型材料.用途广泛的玻璃是一种( )| A. | 金属材料 | B. | 有机合成材料 | C. | 非金属材料 | D. | 复合材料 |
分析 玻璃的主要成分是硅酸盐,属于无机非金属材料,据此进行分析判断.
解答 解:A、玻璃的主要成分是硅酸盐,属于无机非金属材料,不是金属材料,故选项错误.
B、玻璃的主要成分是硅酸盐,属于无机非金属材料,不是有机合成材料,故选项错误.
C、玻璃的主要成分是硅酸盐,属于无机非金属材料,故选项正确.
D、玻璃的主要成分是硅酸盐,属于无机非金属材料,不是复合材料,故选项错误.
故选:C.
点评 本题难度不大,了解玻璃的主要成分是硅酸盐、属于无机非金属材料是正确解答本题的关键.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
6.小亮在做“硫酸中和氢氧化钠溶液”的实验时,滴加硫酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
【查阅资料】Na2SO4溶液呈中性.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
【分析与思考】
(1)溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号).为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuSO4溶液,直到不再产生蓝色沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到硫酸钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入紫色石蕊溶液,若观察到溶液变红色,则所取溶液呈酸性;若不变色,则呈中性.
方案二:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案三:(不能与方案二的原理相同)取样,加入锌粒,若观察到有气泡产生,则所取溶液呈酸性,若无明显现象,则呈中性.
【查阅资料】Na2SO4溶液呈中性.
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
(1)溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号).为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuSO4溶液,直到不再产生蓝色沉淀为止.然后过滤,把滤液倒入蒸发皿中加热,得到硫酸钠晶体.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入紫色石蕊溶液,若观察到溶液变红色,则所取溶液呈酸性;若不变色,则呈中性.
方案二:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案三:(不能与方案二的原理相同)取样,加入锌粒,若观察到有气泡产生,则所取溶液呈酸性,若无明显现象,则呈中性.
7.如图是模拟海水制盐的流程
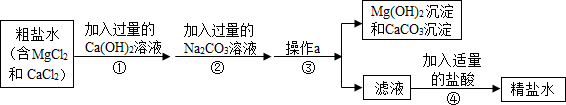
(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若无白色沉淀产生(填实验现象),则证明Ca(OH)2溶液已过量.
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有氢氧化钠 和碳酸钠.
【验证猜想】
【实验结论】经过兴趣小组的实验分析,推出猜想三是正确的.
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O或Na2CO3+2HCl═2NaCl+H2O+CO2↑.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶 操作.
【定量计算】若用上述NaCl晶体配置溶液,取一定质量的该溶液加入足量的AgNO3溶液,所得AgCl沉淀质量等于原NaCl溶液质量.请计算原NaCl溶液中溶质的质量分数.

(1)为了证明第①步所加的Ca(OH)2溶液已过量,某同学取少量①反应后的上层清液,向其中继续加入Ca(OH)2溶液,若无白色沉淀产生(填实验现象),则证明Ca(OH)2溶液已过量.
(2)实验结束后,兴趣小组对滤液进行探究
【提出问题】滤液中除了含有水和氯化钠外,还含有哪些溶质?
【提出猜想】根据实验①②③的操作后,作出如下猜想
猜想一:由于在②中加入了过量的碳酸钠溶液,所以滤液中除了含有水和氯化钠外,还仅含过量的碳酸钠.
猜想二:由于在①加入了过量的氢氧化钙,发生反应生成了氢氧化镁和氯化钙,所以滤液中除了含有水和氯化钠外,只含有反应生成的氯化钙.
猜想三:由于②所加的过量碳酸钠在①之后,所加的碳酸钠把①中反应生成的氯化钙和过量的氢氧化钙全部除去,所以滤液中除了含有水和氯化钠外,还含有氢氧化钠 和碳酸钠.
【验证猜想】
| 步骤 | 实验操作 | 实验现象 | 推断 |
| 1 | 取少量滤液于试管中,加入过量的氯化钙溶液,振荡,静置 | 有白色沉淀生成 | 滤液中还含有碳酸钠 溶质 |
| 2 | 取步骤1反应后的混合液过滤后,取滤液少量于试管中加入 无色酚酞试液 (填指示剂) | 溶液变红色 | 滤液中还含有氢氧化钠 |
【反思与拓展】为了使制得的精盐水只含有水和氯化钠,步骤④的作用是除去杂质,请写出其中一个反应的化学方程式:NaOH+HCl═NaCl+H2O或Na2CO3+2HCl═2NaCl+H2O+CO2↑.如果要将精盐水继续提纯成NaCl晶体,应进行蒸发结晶 操作.
【定量计算】若用上述NaCl晶体配置溶液,取一定质量的该溶液加入足量的AgNO3溶液,所得AgCl沉淀质量等于原NaCl溶液质量.请计算原NaCl溶液中溶质的质量分数.
1.鉴别下列各组物质,所用试剂不正确的是( )
| 选项 | 待鉴别的物质 | 鉴别试剂 |
| A | 铜和黄铜 | 稀盐酸 |
| B | 海水和蒸馏水 | 硝酸银溶液 |
| C | 澄清的石灰水和氢氧化钠溶液 | 二氧化碳 |
| D | 碳酸钠溶液和氢氧化钠溶液 | 无色酚酞试液 |
| A. | A | B. | B | C. | C | D. | D |
8.菜地里绿色蔬菜叶片边缘发黄,小民根据所学化学知识建议父母买化肥改善现状,以获得好收成.他提出买的化肥是( )
| A. | Na2SO4 | B. | CO(NH2)2 | C. | KCl | D. | Ca3(PO4)2 |
6.要验证铜、银、铁三种金属活动性顺序时,不能选用哪组物质进行实验( )
| A. | 银、铜、硝酸亚铁 | B. | 银、铜、铁、硫酸铜 | ||
| C. | 银、铁、硫酸铜 | D. | 铜、硝酸亚铁、硝酸银 |
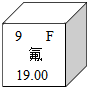 如图所示是氟元素在元素周期表中的相关信息,请回答下列问题:
如图所示是氟元素在元素周期表中的相关信息,请回答下列问题: