题目内容
16. 请根据燃烧条件的探究实验,回答问题:
请根据燃烧条件的探究实验,回答问题:实验目的:验证燃烧需要的条件
实验设计与实施:
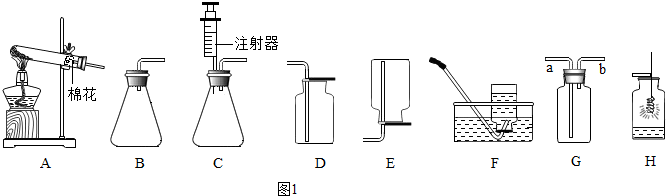
实验一:用棉花分别蘸酒精和水,放到酒精灯火焰上加热片刻,观察现象,发现蘸酒精的棉花燃烧,而蘸水的棉花不燃烧.
实验二:①取一小块乒乓球碎片和滤纸碎片,分别用坩埚钳夹住,放在酒精灯的火焰上加热,观察到乒乓球碎片和滤纸碎片均能燃烧.
②从乒乓球和滤纸上各剪下同样大小的一小片,如图所示放在一块薄铜片的两侧,加热铜片中部,观察现象,发现铜片上的乒乓球碎片比滤纸片先燃烧.
实验三:取两只小蜡烛和一只烧杯,将两只蜡烛分别点燃后平放在实验台上,将其中一只蜡烛用烧杯罩住,观察到(1)蜡烛熄灭.
实验结论:实验一的现象说明,燃烧需要(2)可燃物;实验二中第②步实验中观察到的现象说明乒乓球碎片比滤纸片的着火点(3)低;此实验验证的燃烧的条件是(4)度达到可燃物的着火点.
实验三验证的燃烧的条件是可燃物要与氧气(或空气)接触.
分析 根据燃烧的条件分析,①可燃物 ②氧气或空气 ③达到燃烧所需的最低温度即着火点.
解答 解:实验三:取两只小蜡烛和一只烧杯,将两只蜡烛分别点燃后平放在实验台上,将其中一只蜡烛用烧杯罩住,观察到过一会儿蜡烛将熄灭,可以得出燃烧的条件之一是与氧气接触;
小棉花球蘸水后,因水不可燃,反而会蒸发吸收热量,所以温度达不到棉花的着火点,不会燃烧;而小棉花球蘸酒精后,酒精是可燃物,在酒精灯上被点燃后会燃烧放出大量的热,使温度达到棉花的着火点,引发棉花球燃烧,因此实验一的结论是燃烧的物质必须是可燃物;
滤纸碎片和乒乓球碎片都与氧气接触,在加热过程中,由于乒乓球碎片的着火点较低,首先燃烧起来,说明燃烧需要温度达到可燃物的着火点;
答案:
(1)蜡烛熄灭;(2)可燃物;(3)低;(4)度达到可燃物的着火点;
点评 燃烧的条件是:具有可燃性,与氧气接触,温度达到可燃物的着火点,三者必须同时具备,缺一不可,本实验中,没有涉及氧气是否参加的对比实验,要注意这一点.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
11.下列实验方案正确的是( )
| A. | 用稀硫酸和Cu反应制取氢气 | |
| B. | 用稀盐酸除去CaO中的少量CaC03 | |
| C. | 用水溶解后过滤的方法分离CaCl2和K2C03的混合物 | |
| D. | 用带火星的木条区别氧气和二氧化碳气体 |
1.在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”.如图是他的主要实验步骤,其中操作有误的是( )
| A. |  加入药品 | B. |  收集气体 | ||
| C. |  检查装置的气密性 | D. |  验满 |
6.根据物质的分类知识判断,下列物质属于纯净物的是( )
| A. |  茶饮料 | B. |  矿泉水 | C. |  牛奶 | D. |  蒸馏水 |